
开篇直击:心脏 “阀门” 失灵,全球千万患者盼新解
上海医疗器械博览会了解到,“走路喘、胸口闷、突然头晕”——这些看似普通的不适,可能是重度钙化主动脉瓣狭窄(AS)发出的“求救信号”。作为一种进展迅猛的致命疾病,AS 被称为“心脏瓣膜病中的癌症”,其核心是心脏主动脉瓣因钙化变硬、开合受阻,导致心脏泵血负荷剧增,最终引发心衰、猝死。
数据显示,65岁以上人群中AS发病率超 3%,我国以风湿性病变为主,欧美则以老年性钙化多见。一旦出现症状,未经治疗的患者5年生存率不足50%,50%-70% 最终死于充血性心力衰竭。而传统开胸手术创伤大,很多高龄、高危患者无法耐受,微创的经导管主动脉瓣置换术(TAVI)便成为救命关键——这种“不开胸换瓣膜”的技术,通过血管将人工瓣膜送至病变部位,已让全球数百万患者获益。
重磅消息:FDA 批准!DurAVR 瓣膜全球临床试验启动
就在2025年11月19日,医疗科技公司 Anteris Technologies 宣布:其研发的 DurAVR TAVI 瓣膜,获美国 FDA 批准启动全球多中心临床试验(PARADIGM),正式开启面向重度钙化 AS 患者的疗效验证之路,为未来上市(PMA 申请)铺路。

“这是里程碑式的突破!”Anteris CEO Wayne Paterson 强调,“结合丹麦已启动的试验和首批入组患者,DurAVR将向全球AS患者提供更优的救命选择。”作为一种进展性、致残性疾病,AS的治疗需求迫切,而此次FDA授予的“研究性器械豁免(IDE)”,意味着这款新瓣膜通过了严苛的初期安全性评估,获准进入大规模临床试验阶段。
试验硬核解读:1000 人全球对照,聚焦三大核心终点
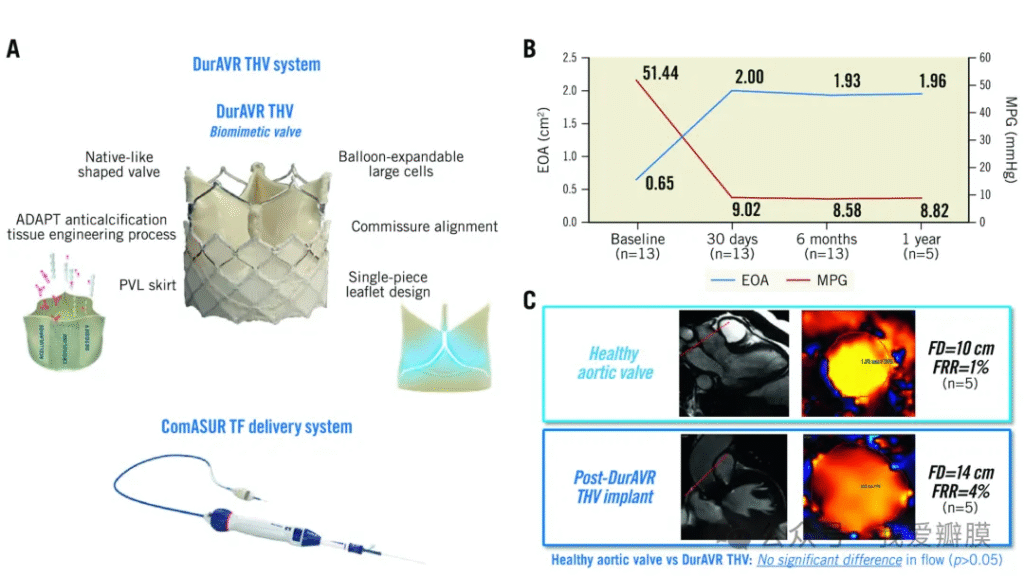
PARADIGM试验的“含金量”,藏在严谨的设计细节里:
1.试验类型:前瞻性随机对照试验(RCT),全球公认的医疗验证“金标准”;
2.覆盖范围:纳入美国、欧洲、加拿大共 1000 名患者,涵盖各类适合 TAVI 治疗的 AS 人群;
3.分组设计:1:1随机分配,一半患者接受DurAVR瓣膜,另一半使用目前已上市的主流TAVI瓣膜,直接“头对头”对比;
4.核心终点:术后1年的“全因死亡+卒中+心血管住院”复合指标,验证DurAVR的非劣效性(即疗效不低于现有标准)。
更值得关注的是,试验由两位心血管领域权威联合主持:美国休斯敦卫理公会医院的Michael J Reardon教授(曾主导多项 TAVI长期随访研究,数据发表于《JACC》),以及瑞士伯尔尼大学医院的 Stephan Windecker 教授,强大的学术背书让试验结果更具说服力。
为什么这件事对患者至关重要?

1.微创治疗再添新选择:TAVI已成为AS治疗的主流,尤其适合无法耐受开胸手术的高龄患者(华西医院数据显示,TAVI手术成功率超98%,最大患者年龄99岁)。DurAVR的加入,将为医生和患者提供更多个性化选择;
2.聚焦钙化难题:重度钙化是TAVI手术的主要挑战,可能导致瓣膜定位困难、并发症风险升高。DurAVR的设计针对性解决这一痛点,有望提升复杂病例的治疗效果;
3.全球数据支撑上市:1000人的大样本、多中心试验,将为DurAVR的安全性和有效性提供扎实证据,加速其获批上市,让全球患者更快受益。
行业展望:TAVI 技术进入 “精准竞争” 时代

随着人口老龄化加剧,AS患病群体持续扩大,TAVI市场迎来快速发展期。此次PARADIGM试验的启动,不仅是Anteris Technologies的重要突破,更标志着TAVI技术从“有无”向“优劣”升级——通过头对头临床试验,推动瓣膜设计优化、疗效提升,最终惠及患者。
对于患者而言,这意味着未来将有更安全、更适配的微创治疗选择;对于医疗行业,这种“以患者为中心”的临床验证,将持续推动心血管介入技术的进步。
目前,PARADIGM试验已在丹麦启动首批患者治疗,美国、欧洲、加拿大的招募工作即将全面展开。让我们期待试验顺利推进,早日为重度主动脉瓣狭窄患者带来新的生命希望!
文章来源:我爱瓣膜。
文章内容仅供知识交流分享使用,如涉侵权请联系我们删除。
