2026年上海医疗器械设计与制造展关注到,心脏计算机断层扫描(Cardiac Computed Tomography, CCT)凭借高各向同性空间分辨率和持续提升的时间分辨率,已成为心脏介入手术规划与引导的重要影像学手段。在电生理介入领域,CCT通过提供精准的解剖学信息,显著改善了心律失常治疗的安全性与有效性,尤其在房颤消融、左心耳封堵(Left Atrial Appendage Occlusion, LAAO)、室性心动过速(Ventricular Tachycardia, VT)消融等关键治疗中发挥核心作用。本文结合最新临床研究与技术进展,系统阐述CCT在电生理介入全流程(术前评估、术中引导、术后随访)中的应用价值,并探讨其与新兴技术的融合前景。
CCT在房颤(Atrial Fibrillation, AF)消融中的应用
房颤作为最常见的持续性室上性心律失常,其导管消融治疗的成功高度依赖术前解剖评估与术中精准定位。CCT凭借多维度优势,成为房颤消融围手术期的关键影像学工具。
(一)术前评估:排除血栓与解剖可视化
1. 左心耳(Left Atrial Appendage, LAA)血栓排查
经食管超声心动图(Transesophageal Echocardiography, TEE)是评估LAA血栓的金标准,但CCT在排除血栓方面表现出极高的可靠性。动脉期CCT中,LAA血栓表现为低衰减的造影剂充盈缺损,而延迟期(30-180秒)扫描可有效区分血栓与血流缓慢——血栓在延迟期仍保持充盈缺损,血流缓慢则随造影剂混匀而消失。研究显示,结合延迟期扫描的CCT诊断LAA血栓的敏感性达100%、特异性99%、阴性预测值(NPV)100%,且相比TEE能缩短检查时间与患者等待时间,提升就医体验。
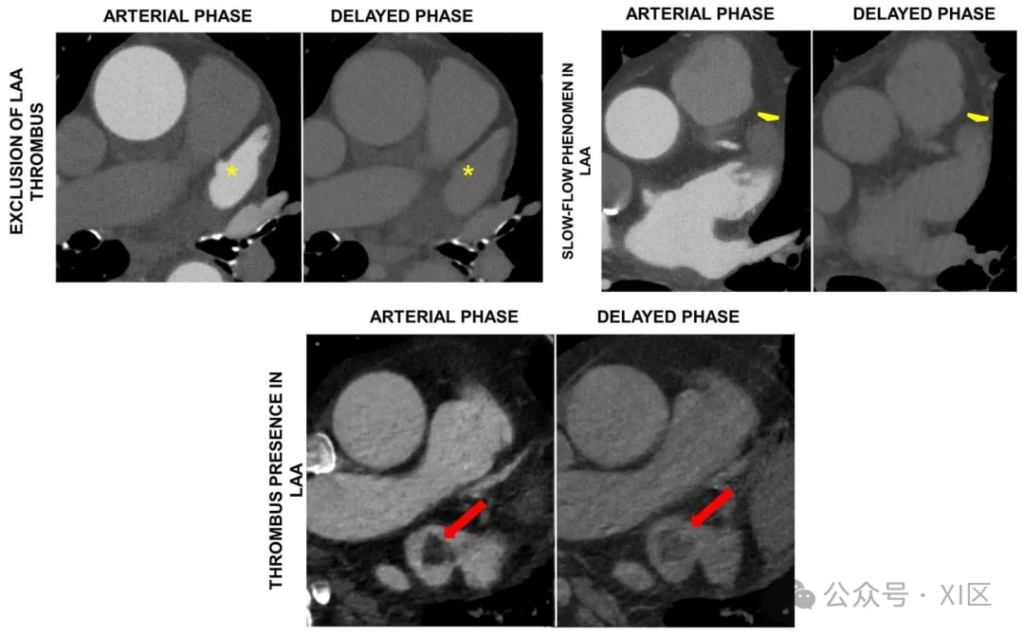
采用心脏计算机断层扫描(CCT)对拟行肺静脉隔离术的房颤患者进行左心耳(LAA)评估,分别展示动脉期(左图)与延迟期(右图)成像结果。左上图为左心耳无血栓的典型案例,两期成像均显示正常造影剂强化;右上图为左心房严重扩大患者的慢血流现象案例,动脉期左心耳远端部分造影剂分布不均且强化缺失,而延迟期左心耳则呈均匀造影剂充盈。下图为左心耳迁移性血栓案例,动脉期左心耳近端出现充盈缺损,且该缺损在延迟期成像中持续存在 。
2. 心房与肺静脉(Pulmonary Vein, PV)解剖评估
CCT可清晰显示左心房(Left Atrium, LA)大小、PV开口形态及变异(如副PV、共干PV),其测量结果与心腔内超声、电解剖标测(Electroanatomical Mapping, EAM)高度一致。此外,CCT能精准勾勒LA、PV与食管、膈神经的解剖关系:通过明确食管走行,可个性化规划消融线以降低食管损伤风险;通过重建心包膈血管束,可定位膈神经位置,减少消融相关膈神经损伤。
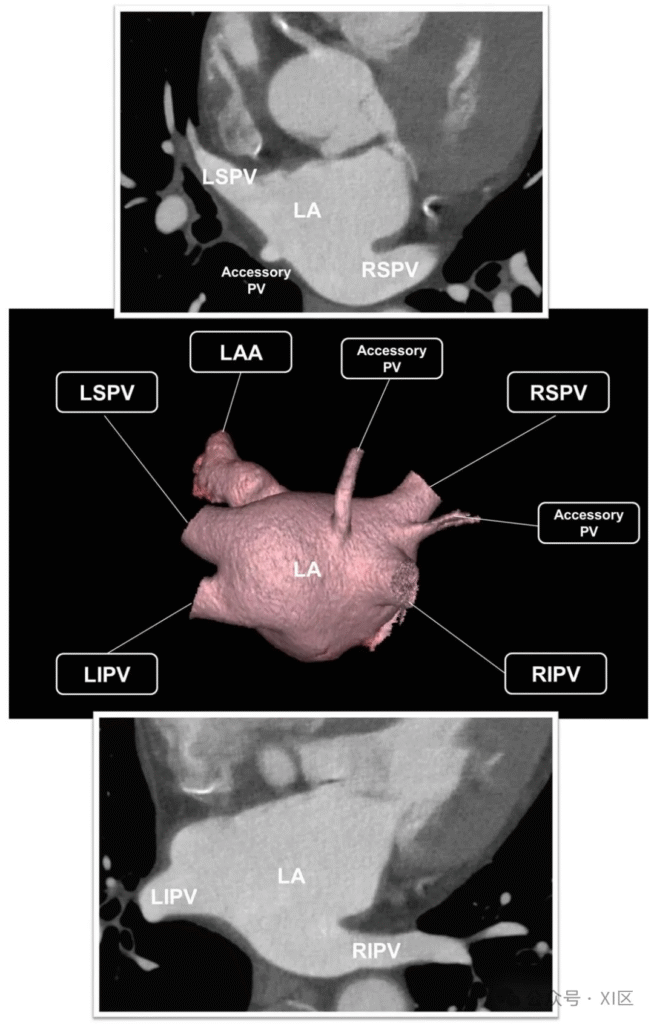
通过心脏计算机断层扫描(CCT)的轴位图像与三维重建技术显示左心房(LA)和肺静脉(PV)的解剖结构。最常见的解剖结构为左心房后部存在四个独立的肺静脉开口:右侧肺静脉中,右上肺静脉(RSPV)与右下肺静脉(RIPV)分别开口,且常被左心房壁分隔;左侧肺静脉中,左上肺静脉(LSPV)与左下肺静脉(LIPV)开口位置通常较为接近,无明显分隔结构。副肺静脉指与同侧上、下肺静脉分开并单独汇入左心房的肺静脉,其命名通常依据所引流的肺段,在人群中的发生率高达 25%,且右侧发生率高于左侧。若存在副肺静脉,其主干通常比主肺静脉更短、管腔更窄,有时可能跨越肺裂 。
3. 消融预后预测因素评估
CCT可量化左心房壁厚度、心外膜脂肪体积与密度,这些指标与房颤消融复发密切相关。例如,左心房壁厚度>3.10mm提示消融反应不佳;心外膜脂肪密度增加及分布异质性是房颤复发的独立危险因素。术前基于CCT的解剖特征分析,有助于筛选适合消融的患者并优化治疗策略。
(二)术中引导:影像整合与精准定位
CCT的三维(3D)重建图像可与EAM系统融合,实现“解剖-电生理”双导航。通过分割LA、PV等目标结构,并与EAM标测的内膜轮廓对齐,医生可实时调整消融导管位置,确保肺静脉隔离的完整性。单中心研究与随机试验显示,这种影像整合技术能提高长期窦性心律维持率,但不同研究间的疗效一致性仍需进一步验证。
(三)术后随访:并发症诊断与管理
房颤消融后常见并发症包括肺静脉狭窄(Pulmonary Vein Stenosis, PVS)与心房食管瘘(Atrioesophageal Fistula, AEF)。CCT是诊断PVS的首选手段,可通过对比术前术后影像量化狭窄程度(轻度<50%、中度50%-70%、重度>70%),并指导球囊扩张或支架植入。对于罕见但致命的AEF,CCT通过口服造影剂可清晰显示食管穿孔与造影剂外溢,为紧急干预争取时间。
CCT在左心耳封堵(LAAO)中的核心价值
对于卒中风险高且无法长期抗凝的房颤患者,LAAO是预防系统性血栓栓塞的重要替代方案。CCT在LAAO的术前规划、术中引导与术后并发症监测中均展现出不可替代的作用。
(一)术前规划:解剖评估与器械选择
1. LAA形态与尺寸测量
CCT可精准分类LAA形态(鸡翅型、仙人掌型、风袋型、菜花型),不同形态与手术难度及卒中风险相关:鸡翅型占比最高(48%),虽手术复杂度高但卒中风险最低;菜花型占比仅3%,却因结构不规则导致器械植入困难,卒中风险是鸡翅型的8倍。此外,CCT通过二维斜轴位测量LAA开口直径与着陆区长度,为封堵器尺寸选择提供依据,其测量准确性优于TEE。
2. 关键解剖关系评估
CCT可清晰显示LAA与左肺静脉、左回旋支动脉、膈神经等邻近结构的关系,避免术中损伤。例如,左肺静脉常作为输送鞘的锚定结构,CCT对其位置的评估直接影响穿刺路径选择;对于“反向鸡翅型”LAA,CCT可指导选择更靠前的房间隔穿刺点,提高手术成功率。
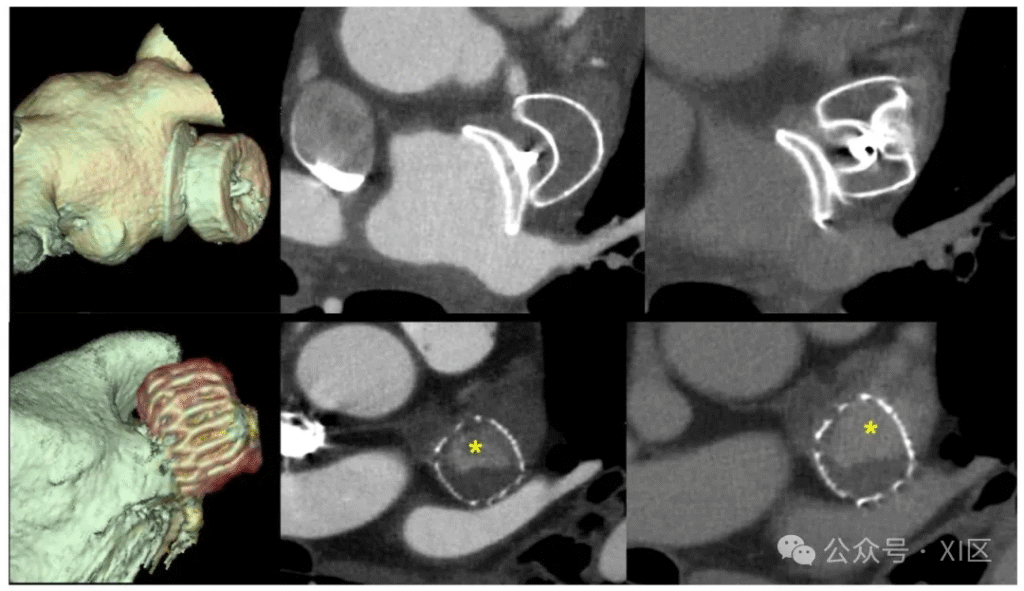
(二)术中与术后:引导与并发症监测
术中CCT数据可与血管造影图像融合,提供实时解剖导航,减少造影剂用量与辐射暴露。术后CCT是监测并发症的金标准:
- 器械相关血栓(Device-Related Thrombus, DRT):表现为封堵器心房面的低衰减增厚区域;
- 瓣周漏(Peri-Device Leak, PDL):根据漏口大小分为轻微(<1mm)、轻度(1-3mm)、中度(4-5mm)、重度(>5mm),CCT敏感性优于TEE;
- 器械侵蚀:虽罕见,但CCT可早期发现封堵器穿透LAA壁的迹象,避免心包填塞等严重后果。
CCT在室性心动过速(VT)消融中的技术突破
VT是结构性心脏病(如冠心病、心肌病)患者猝死的主要原因,导管消融的关键在于精准定位致心律失常病灶。CCT通过心肌瘢痕与解剖结构评估,为VT消融提供重要指导。
(一)术前评估:排除血栓与定位病灶
1. 左心室(Left Ventricle, LV)血栓排查
CCT在排除LV血栓方面优于经胸超声,与心脏磁共振(Cardiac Magnetic Resonance, CMR)相当,尤其适用于体内有金属植入物(如起搏器)无法行CMR的患者。延迟期CCT中,血栓表现为持续的低衰减区,而正常心肌则均匀强化。
2. 心肌瘢痕与病灶定位
在缺血性心肌病患者中,CCT可通过延迟增强扫描识别心肌瘢痕,其显示的室壁变薄区域(<5mm)与EAM中的低电压区(<1.5mV)高度吻合,可直接指导消融靶点选择。对于非缺血性心肌病,新型技术如光谱CCT与晚期碘增强(Late Iodine Enhancement, LIE)可改善瘢痕识别准确性,为VT病灶定位提供新途径。
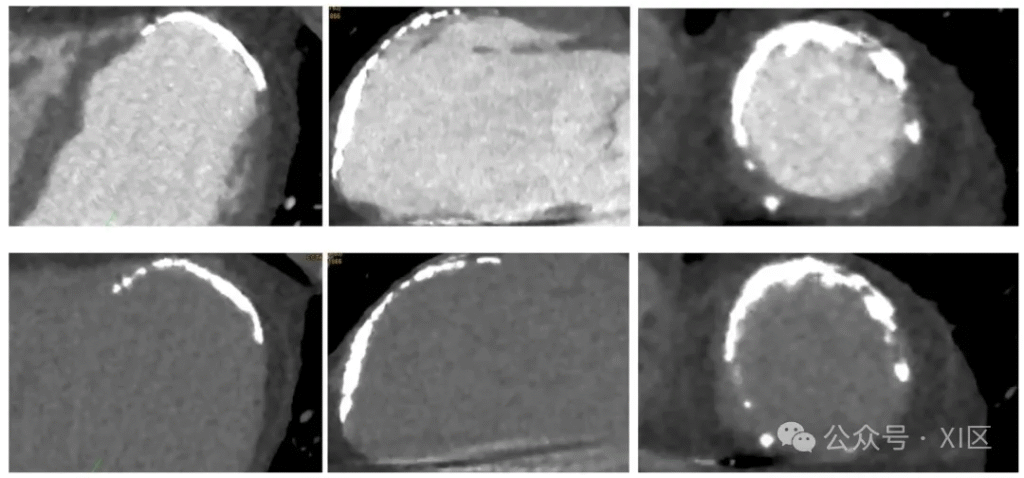
心脏计算机断层扫描(CCT)在室性心动过速(VT)消融中的应用。一名 55 岁缺血性心肌病患者,有广泛心肌梗死病史,为排除左心室(LV)血栓接受 CCT 检查。上图展示左心室的三腔心、两腔心及短轴位增强 CCT 图像;下图为延迟期成像,左心室心尖部、前壁及前间隔部心肌存在严重钙化且运动消失,但造影剂呈均匀强化,可安全排除血栓。该增强 CCT 图像在围手术期用于指导消融操作 。
(二)术中引导与技术创新
CCT的3D心脏模型可与EAM系统整合,帮助医生聚焦瘢痕区域进行高分辨率标测,减少手术时间与辐射暴露。此外,光子计数探测器CT(Photon-Counting Detector CT)的出现显著提升了光谱成像质量,可通过单次延迟扫描计算细胞外容积分数,量化心肌纤维化程度,为VT消融疗效评估提供量化指标。
CCT在其他电生理介入中的应用
(一)心脏再同步治疗(Cardiac Resynchronization Therapy, CRT)
CCT通过静脉期成像评估冠状静脉系统解剖,包括冠状窦、心中静脉及侧后静脉,为左心室电极植入路径规划提供依据。研究显示,基于CCT的多模态影像引导可提高电极植入准确性,降低CRT无应答率(目前无应答率约30%)。
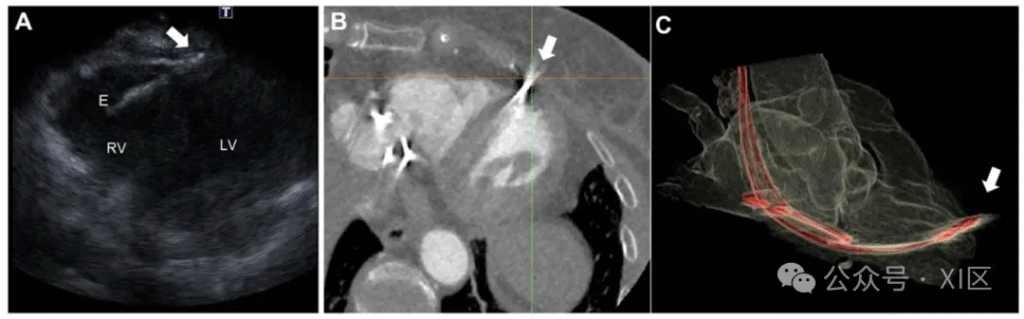
心脏计算机断层扫描(CCT)在心脏植入式电子器械(CIED)评估中的应用。一名 63 岁女性患者,10 年前因病态窦房结综合征植入双腔起搏器,1 年前因气胸接受起搏器翻修术,此次因膈肌及胸壁肌肉刺激症状就诊。临床检查与心电图未见明显异常;经胸超声心动图显示左右心室收缩功能正常,但提示右心室心肌可能存在穿孔(A 图)。CCT 进一步证实右心室起搏器电极位于心肌外(B 图、C 图),同时显示起搏器导线及胸壁骨骼结构,并发现心包存在少量积液。最终患者接受右心室电极拔除术并植入新起搏器 。
(二)器械拔除
对于感染或故障的心脏植入电子器械(如起搏器、除颤器),术前CCT可评估静脉通畅性、导线粘连与穿孔情况,预测拔除难度。CCT识别的严重导线粘连与复杂拔除术及并发症风险显著相关,可为手术策略制定提供关键参考。此外,CCT生成的混合现实全息影像可在术中实时导航,进一步提高拔除安全性。
CCT的局限性与未来展望
(一)现存挑战
CCT的主要局限性包括辐射暴露(尤其多次延迟扫描时)、碘造影剂相关肾损伤风险,以及快速心室率房颤患者中的运动伪影问题。此外,在非缺血性心肌病的瘢痕评估中,CCT仍逊于CMR,需进一步技术优化。
(二)未来方向
1. 技术融合:CCT与人工智能(AI)的结合将实现自动化解剖分割与病灶识别,缩短影像后处理时间;与3D打印技术结合可生成个性化心脏模型,用于术前模拟与手术培训。
2. 功能成像升级:光子计数CT与定量灌注成像技术将进一步提升心肌功能与纤维化评估能力,实现“解剖-功能”一体化成像。
3. 无辐射替代探索:虽目前CCT仍依赖电离辐射,但未来基于深度学习的低剂量成像算法有望在保证图像质量的同时降低辐射剂量。
结语
心脏计算机断层扫描(CCT)已从单纯的解剖成像工具发展为电生理介入治疗的“全程伴侣”,在房颤消融、左心耳封堵、室性心动过速消融等领域的术前评估、术中引导与术后随访中发挥核心作用。随着与AI、3D建模、光子计数探测等技术的深度融合,CCT将进一步突破现有局限,为精准电生理治疗提供更全面的影像学支持,最终改善心律失常患者的预后。
文章来源:XI区。
文章内容仅供知识交流分享使用,如涉侵权请联系我们删除。
