2026上海医疗器械展览会|国内脉冲电场消融技术全景分析:从技术突破到未来演进
2026上海医疗器械展览会了解到,脉冲电场消融(Pulsed Field Ablation, PFA)作为心脏电生理领域近十年来最具颠覆性的创新技术,正在从根本上改变房颤等心律失常的治疗范式。本文基于国家药品监督管理局官方数据、企业公开信息、临床研究文献及行业分析报告,对国内PFA技术进行系统性梳理。文章首先阐释PFA区别于传统热消融的核心技术原理与组织选择性优势;其次,详细盘点截至2026年初已获批的国产PFA产品,从技术路线、临床数据、产品特点等维度进行对比分析;再次,对当前市场竞争格局与市场份额分布进行深入剖析;最后,从波形优化、三维整合、适应症拓展、联合治疗及智能化等方向,解析PFA技术的未来演进路径。本文旨在为医疗器械行业从业者、临床医生及政策制定者提供一份全面、深入、前瞻的参考。
2026年上海医疗器械展|弹簧圈栓塞微导管比较
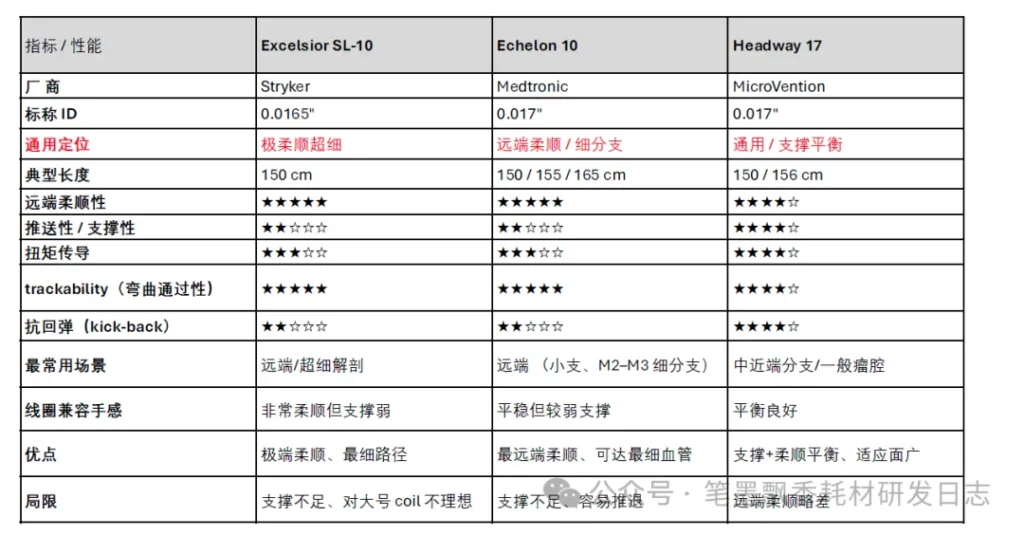
2026年上海医疗器械展关注到,微弹簧圈应用历史悠长,主要应用于脑动脉瘤、胃肠道出血、外周血管性疾病等,近年来也用于冠状动脉穿孔栓塞治疗。
Medtec上海展|导管哪家强?一文看懂神经介入导管的结构秘密与设计逻辑

Medtec上海展了解到,我们或许也曾困惑:为什么有的微导管能轻松进入远端血管,而有的却频频“卡脖”?为什么看似相同尺寸的导管,操控性能却大相径庭?
上海医疗器械博览会|介入科常用栓塞材料及适应证

上海医疗器械博览会了解到,介入科常用的栓塞材料种类繁多,选择取决于治疗目的(如止血、灭活肿瘤)、目标血管的大小、以及需要栓塞的持久性。下面按主流分类方式,为你梳理常用材料及其核心适应证。
2026年上海医疗器械设计与制造展|一文解析导鞘及导引导管
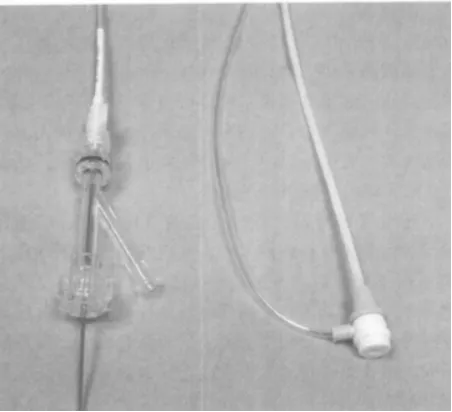
2026年上海医疗器械设计与制造展了解到,术中当穿刺针与导丝完成血管穿刺后,术者需确保血管通路通常有效。如操作仅为诊断目的,则无需频繁更换多种导管导丝,仅使用单一导丝搭配相应诊断导管,即可使穿刺点伤口最小化。此方法无需通过一次或多次更换猪尾导管,就能完成灌注式主动脉造影(或腔静脉造影)并获取所需影像。
上海医疗器械博览会|医疗挤出管模具设计全解析(单腔管篇)

上海医疗器械博览会了解到,医疗导管(如导引导管,微导管,泌尿导管等)产品性能与单腔挤出管的精密性息息相关,而单腔管的精密性核心依赖挤出模具设计,本文将剥离挤出模具的复杂外壳,聚焦核心零件的设计本质
—芯模(定内径)与 口模(控外径) 的设计。(注:本文不涉及模体、分流器等其他模具部件。)
上海医疗器械展|医用显示器性能稳定性研究及监管建议
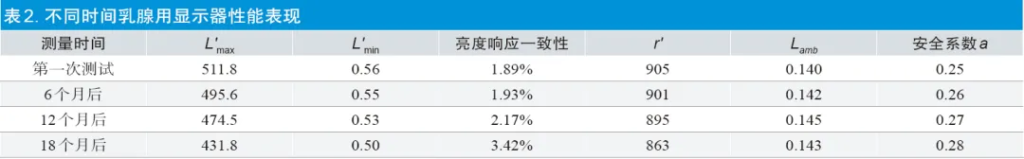
上海医疗器械展关注到,医用显示器作为医学影像诊断的关键终端设备,其性能稳定性直接影响临床诊断准确性。文章分析了影响医用显示器性能稳定性的关键指标,包括亮度、灰阶一致性等参数的变化规律,并研究了长期使用可靠性和系统稳定性对诊断效果的影响。同时,探讨了医用显示器性能稳定性的评估方法。结合国内外监管要求,提出了完善标准体系、加强全生命周期监管、提升行业认知等三条建议,旨在提高医用显示器的临床使用安全性和诊断准确性。
2026上海医疗器械展览会|强到没朋友,却难倒工程师:塑料王PTFE的两副面孔

2026上海医疗器械展览会了解到,塑料王,PTFE,聚四氟乙烯(学名),也叫铁氟龙,一般是白色。第一次接触到这个PTFE,是聚四氟乙烯垫片,用来密封使用的。后面再次接触,就是e-PTFE膜、PTFEliner、PTFE线、PTFE管,没错就是医疗器械产品上常见的,血管支架的覆膜材料、复合管的内衬和PTFE缝合线。
Medtec上海展|透视生命,孪生未来:CT与数字孪生技术如何重塑现代医学

Medtec上海展关注到,在人类认知自我、探索生命奥秘的漫长征程中,我们始终渴望拥有一双能够穿透皮肤与骨骼,直视内部结构与功能的“神之眼”。这一梦想,随着计算机断层扫描(CT)与磁共振成像(MRI)技术的诞生与发展,已然成真。它们如同两位技艺超群但又各有所长的画师,一位精于勾勒人体的“骨骼大厦”与“形态疆域”,另一位则擅长描绘组织的“水质画卷”与“功能密码”。而今天,一项源于工业界的概念——数字孪生,正携带着CT与MRI提供的海量数据,试图为每一个人创建一个动态、高保真的虚拟化身。这不仅仅是静态的影像,更是一个可以模拟、预测、干预的生命系统模型。
2026年上海医疗器械设计与制造展|智能化、精准化、专科化、协同化,MEDICA现场医疗机器人还有哪些看头?

2026年上海医疗器械设计与制造展了解到,医疗机器人行业是融合机器人技术、人工智能与临床医学的高端医疗装备领域,目前正处在高速发展期。根据应用场景,医疗机器人主要可分为手术机器人、康复机器人、辅助机器人等类别。它们凭借清晰的成像系统、高自由度的机械臂和智能算法,正在外科手术、康复训练、医院物流、慢病管理等众多诊疗环节中发挥重要作用。
