FDA进一步关切人工智能
FDA新近批准了中风检测软件,这为人工智能在医疗保健领域应用的蓬勃发展铺平了道路。
FDA医疗器械注册,分五步走!
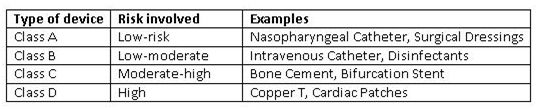
医疗器械在美国上市前的第一个步骤就是依据联邦法规对器械进行分类。联邦食品、药品以及化妆品法案(FD&C Act)201(h)部分对医疗器械进行了定义,在联邦法规中可以看到对器械的分类,
【学术分享】植入式神经刺激器新版标准浅析
植入式神经刺激器是以一定程度的电流脉冲刺激靶点神经,以调整或恢复脑部、神经或肌肉功能,使症状缓解的一种方法。
《修正案草案》完善医疗器械上市许可持有人制度等内容
2017年10月1日,中共中央办公厅、国务院办公厅印发《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(以下简称《创新意见》),提出36项重要改革措施。
阅读更多
境内外法规检查的过程比较, 对中国制造业准备FDA检查的启示
无论是FDA对中国制造业的检查,还是CFDA的海外检查,对于检查和被检查的双方来说都有一个认知和熟悉的过程,这个过程的长短几乎可以决定检查过程是否能够顺利得进行,很大程度上也决定了检查结果的好坏。
阅读更多
“欧美准备CFDA检查”带给“中国制造商准备FDA检查”的启示
018年在年初经历了美国政府停摆,FDA取消检查,过门而不入,让中国制造商进不是,退也不得的尴尬境地之后, 最近有机会替欧美的顶级制造商准备将要到来的中国FDA的检查,

中国实施国际统一的唯一器械标识(UDI) 进一步促进全球范围的医疗器械上市后监管
为了加强医疗器械全球上市后监管,促进追溯管理效率提高,全球形成了唯一器械标识(UDI)的协调方案,美国和欧洲也都开始进入实施准备阶段。针对中国地区如何实施的问题,文章介绍了UDI的产生和建立的基本原则,比较了国内药品电子监管实施的差异,提出通过走国际化协调的道路,来解决中国医疗器械UDI的实施,更有利于中国监管和产业发展。

印度医疗器械监管重点
本文分析了印度《医疗器械法规2017》的主要特点,旨在探讨其对印度医疗器械行业发展的影响。
浅析医疗器械产品技术要求
文章介绍了医疗器械产品技术要求的产生,产品技术要求与产品注册标准的区别。梳理了产品技术要求所涉及的医疗器械各个环节,分析讨论了医疗器械产品技术要求对于整个医疗器械全周期的重要性。
阅读更多
器审中心公开8个技术审评报告
为了全面贯彻落实国务院《关于改革药品医疗器械审评审批制度的意见》(国发〔2015〕44号)文件精神,提高审评审批透明度,器审中心自2017年12月至2018年4月,共公开8份《医疗器械产品技术审评报告》。
阅读更多
