盛禧奥成功通过ISO 13485: 2016 认证,全力支持医疗行业的质量和安全发展
盛禧奥,全球塑料、胶乳胶粘剂和合成橡胶材料生产商,其全球所有医疗树脂生产基地及相关部门,在2016 年底达致了一个新的里程碑— 成功取得ISO13485:2016 认证

权威解读IVD注册流程与申报材料要求(质量管理人士必读!)
医疗干货群邀请到了现任中国食品药品检定研究院体外诊断试剂检定所副研究员胡泽斌医学博士,为大家分享体外诊断试剂注册法规与流程简介。
阅读更多
医械优先审批申报怎么写?CFDA给出了一份指南
2月15日,国家食品药品监督管理总局(CFDA)发布了《医疗器械优先审批申报资料编写指南(试行)》,旨在进一步做好医疗器械优先审批申报资料编写工作。
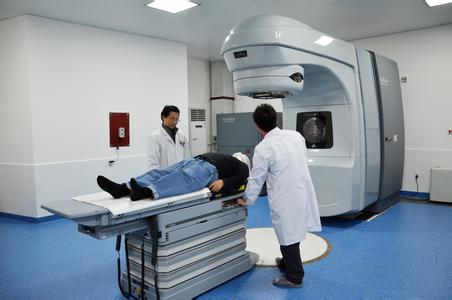
安徽印发第一类医疗器械产品备案管理新规
安徽省局印发此《办法》,明确监管部门职责及备案人主体责任,并对备案事项的变更、信息管理与公示、事后监管等做出详细规定。
你应知道的2016年FDA发布的指导文件
2016年,美国FDA又发布了若干指导性文件,这些文件对组合生产力和策略部署有实质性的积极影响,以下这些指导文件值得每一个医疗器械制造者细心考虑。

CFDA发布医疗器械审评沟通交流管理办法
为贯彻实施《国务院关于改革药品医疗器械审评审批制度的意见》(国发〔2015〕44号)、《创新医疗器械特别审批程序(试行)》(食药监械管〔2014〕13号)及《医疗器械优先审批程序》(国家食品药品监督管理总局公告2016年第168号),国家食品药品监督管理总局组织制定了《医疗器械审评沟通交流管理办法(试行)》(附件),现予发布。
阅读更多
医疗器械质量管理体系最新版标准正式发布,将于今年5月起实施
2017年1月19日,国家食品药品监督管理总局发布YY/T0287-2017 /ISO13485:2016《医疗器械 质量管理体系 用于法规的要求》标准,将于2017年5月1日起实施。
阅读更多
YY/T0287-2017《医疗器械 质量管理体系 用于法规的要求》标准正式发布
2017年1月19日,国家食品药品监督管理总局发布YY/T0287-2017 /ISO13485:2016《医疗器械 质量管理体系 用于法规的要求》标准,将于2017年5月1日起实施。
烟台启动六个月医疗器械说明书和标签专项检查
烟台市食药监局近日启动为期六个月的医疗器械说明书和标签专项检查。市食药监局医疗器械科工作人员杜亚妮:“本次检查分为企业和使用单位自查整改、全面检查和市局督导抽查三个阶段,将对我市医疗器械生产企业、实施三级监管的医疗器械经营企业和全市二级以上医疗机构所生产、经营和使用的医疗器械产品进行检查。”
阅读更多
总局关于发布医用磁共振成像系统临床评价等4项医疗器械注册技术审查指导原则的通告(2017年第6号)
为加强医疗器械产品注册工作的监督和指导,进一步提高注册审查质量,国家食品药品监督管理总局组织制定了《医用磁共振成像系统临床评价技术审查指导原则》《口腔颌面锥形束计算机体层摄影设备注册技术审查指导原则》《体外除颤产品注册技术审查指导原则》《光固化机注册技术审查指导原则》(见附件),现予发布。
阅读更多