上海医疗器械博览会关注到系统回顾冠状动脉药物涂层球囊(DCB)在冠心病介入治疗中的发展历程、作用机制、核心适用范围与扩展应用。DCB通过“无植入”策略,避免永久金属支架带来的血栓与再狭窄风险,已在支架内再狭窄(ISR)治疗中确立有效性,并在小血管病变、分叉病变、弥漫长病变、急性冠脉综合征(ACS)、糖尿病与高出血风险人群中展现出广阔潜力。多项随机研究与真实世界数据表明,DCB在特定适应症下可与药物支架(DES)疗效相当甚至优于DES。DCB治疗效果高度依赖病变准备质量,强调使用影像指导、非顺应球囊、切割球囊或旋磨等策略。尽管当前仍需更多高质量前瞻性研究来验证其在非ISR病变中的长期安全性与有效性,但DCB正逐步成为冠脉介入治疗中的重要工具。
背景介绍
导管介入治疗的发展已经彻底改变了冠状动脉疾病(CAD)的治疗方式,从1929年的首次心脏导管插入术到药物涂层球囊(DCBs)作为支架内再狭窄(ISR)治疗方法的出现。本综述探讨了DCBs在CAD中的演变和临床应用,特别关注其在管理ISR、de novo冠状动脉疾病和复杂病变中的作用。
DCBs向血管壁输送抗增殖药物,如紫杉醇或西罗莫司,并已成为传统支架疗法的有前景的替代方案,减少了永久性金属植入物的需求及相关血栓风险。早期研究证明了DCBs在ISR中的有效性,而近期研究已将其应用扩展到小血管疾病、分叉病变和长弥漫性病变。值得注意的是,在某些情况下,包括高风险患者和那些具有复杂冠状动脉解剖结构的患者,DCBs已显示出与药物洗脱支架(DES)的非劣效性。尽管存在一些挑战,如冠状动脉夹层的可能性和需要最佳病变准备,但DCBs在减少各种患者群体的再狭窄和改善长期结局方面显示出强大潜力。虽然需要进一步研究以优化其在超适应症应用中的使用,但DCBs可能代表了一种多功能、有效且更安全的CAD管理方法。
历史概述
1929年,德国医生Werner Forssman首次在人类身上进行了导管插入术,他使用导尿管对自己进行了右心导管插入术。1963年,Charles Dotter医生对狭窄的右髂动脉进行了首次经腔血管成形术,奠定了基于导管的闭塞性动脉疾病经皮治疗的基础。1974年,Andreas Gruntzig医生描述了“Gruntzig球囊导管原理”,其中使用双腔导管施加均匀压力10至30秒,将动脉粥样硬化斑块压缩 against 血管壁并恢复血流。这被称为“经皮冠状动脉腔内成形术”。1977年,他首次在人类身上进行了冠状动脉球囊扩张术。这已发展成为心血管医学中最成功的治疗干预措施之一。
除了球囊扩张术,Dotter于1964年首次描述了血管内“夹板”的概念,并建议使用非生物性血管内支架来稳定病变动脉血管。第一枚冠状动脉支架于1986年3月28日由法国图卢兹的Jacques Puel医生植入患者体内。冠状动脉支架领域也经历了巨大发展,得益于Cesare Gianturco医生、Gary S. Roubin医生、Julio Palmaz医生和Richard A. Schatz医生的努力,他们都对球囊扩张支架的发展做出了重要贡献。
为什么选择药物涂层球囊?
使用普通球囊血管成形术(POBA)、裸金属支架(BMS)或药物洗脱支架(DES)的经皮冠状动脉介入治疗(PCI)是冠状动脉疾病的首选侵入性治疗。但仍存在局限性,例如BMS的支架内再狭窄和POBA的再狭窄。因此,即使对于第二代DES,一个持续关注的问题是晚期新生动脉粥样硬化和血栓事件的晚期发生(第一年支架内再狭窄发生率为6-8%),以及每年2%的不良缺血事件发生率,且无明显平台期。此外,这些不良事件在某些情况下更常见,例如小血管疾病和具有大狭窄侧支的复杂冠状动脉分叉病变。因此,药物涂层球囊(DCB)作为一种有吸引力的替代方案出现,实现了“不留异物”策略,消除了永久性金属假体带来的升高血栓风险和延长双抗血小板治疗(DAPT)导致的出血风险增加。
药物涂层球囊
在1990年代末,德国蒂宾根的一个研究小组研究了紫杉醇暴露对动脉壁的影响,证明了其对新生内膜形成的剂量依赖性抑制。同时,Ulrich Speck和Bruno Scheller医生证明,对比剂的使用可作为紫杉醇的载体,促进其转移到血管壁。这些经验为DCB的诞生奠定了基础,其中快速交换半顺应球囊导管涂有活性抗增殖物质——主要是紫杉醇,最近还有西罗莫司——以及一种载体,可以允许快速药物摄取及其在血管壁中的持久存在以抑制新生内膜形成。图1描述了DCB在血管壁中的作用机制。
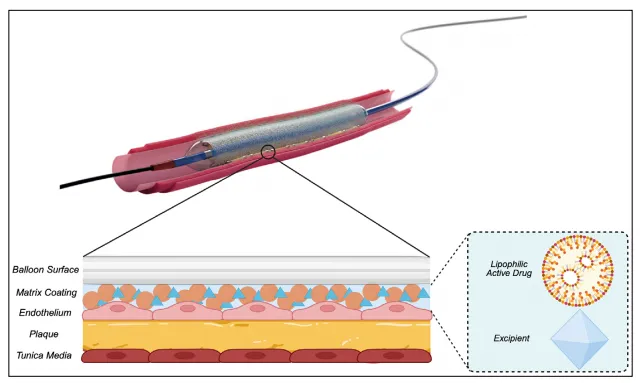
图1 药物涂层球囊的作用机制。
在有效的DCB技术中,应考虑几个生物学和程序因素。抗增殖剂可分为两种主要药物:紫杉醇和西罗莫司。紫杉醇是一种众所周知的强效抗肿瘤剂,通过不可逆地结合微管并增强微管组装起作用,导致有丝分裂期间细胞复制受阻。因此,有报道描述紫杉醇具有通过仅DCB治疗后晚期管腔增加而产生积极重塑效应。此外,紫杉醇是一种高亲脂性剂,能够快速细胞摄取,并以最小剂量维持持续生物效应。
另一方面,西罗莫司,也称为雷帕霉素,具有强抗增殖和免疫抑制特性。它通过结合细胞内胞质蛋白FK结合蛋白-12,形成复合物并可逆地抑制哺乳动物雷帕霉素靶标(mTOR)的激活,导致细胞周期在G1/S转换处停滞。西罗莫司存在某些局限性,如转移率差和组织中滞留时间延长。尽管如此,紫杉醇涂层球囊(PCB)和西罗莫司涂层球囊具有可比的临床和血管造影治疗效果。
赋形剂是非活性成分,在活性药物递送和改善与血管壁的相互作用中起主要作用。临床验证的载体有碘普罗胺(一种低渗对比剂)和尿素(一种内源性代谢物)。这些载体改善药物粘附和滞留,以保证 prolonged 治疗效果。
开发独特的涂层系统对于优化药物递送至关重要。球囊涂层特性为药物释放动力学、粘附特性和整体疗效提供了优势。涂层特征,如在整个表面积上具有均匀厚度和药物浓度,以及球囊膨胀时涂层破碎成亚微米颗粒,对于增强亲脂性药物向血管组织的转移能力很重要。涂层成分在不同设备间显著不同,外观从树脂状到多层和结晶状各异。一种新的纳米封装涂层方法可能提供更好的药物溶解度和稳定性,并通过控释增强药物递送。然而,需要更稳健的临床数据来推动该技术向前发展。
由于药物类型、配方、转移动力学和生物利用度的差异,DCBs不被认为具有类效应,因为不同DCB选项之间存在疗效和安全性特征的差异。图2突出了紫杉醇和西罗莫司DCB之间的主要差异。
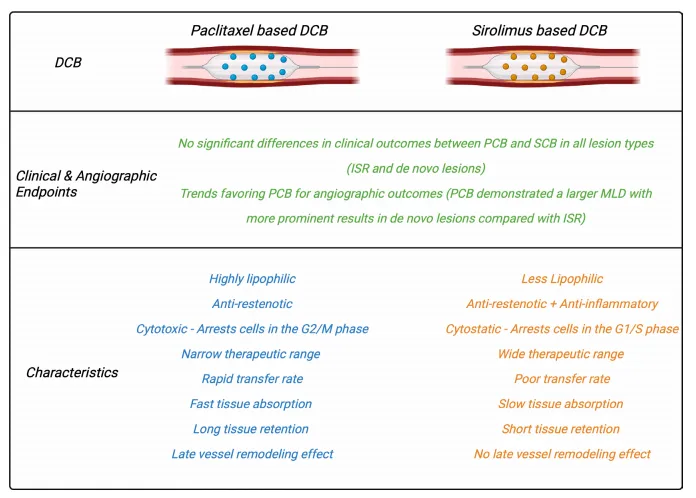
图2 紫杉醇与西罗莫司药物涂层球囊的主要特性及差异
DCB:药物涂层球囊;PCB:紫杉醇涂层球囊;SCB:西罗莫司涂层球囊;ISR:支架内再狭窄;MLD:平均管腔直径
支架内再狭窄
随着1990年代末BMS的引入,出现了一种新的临床实体:支架内再狭窄(ISR)。ISR在血管造影上定义为先前支架段内或支架边缘邻近(近端和远端边缘5 mm内)管腔直径减少>50%。组织学上,ISR是一个由夸张的新生内膜组织变化引起的负性血管重塑缓慢过程。这些变化特征为早期ISR,主要由新生内膜增生引起,和晚期ISR,由新生动脉粥样硬化引起。尽管支架技术的进步降低了ISR风险,但它仍然是PCI失败的主要原因,占美国所有PCI手术的5%至10%。因此,制定预防和优化管理ISR的策略至关重要。
表1突出了展示DCBs在ISR中性能的主要随机对照试验(RCTs)。AGENT IDE(评估Agent紫杉醇涂层PTCA球囊导管治疗支架内再狭窄受试者的临床试验)试验在混合ISR中突出了DCB治疗策略优于POBA。该研究的1年结果显示,与POBA组相比,靶病变失败(TLF)、靶病变血运重建(TLR)和靶血管相关心肌梗死显著减少,使得美国食品药品监督管理局批准AGENTTM DCB(波士顿科学公司)用于ISR。最近,AGENT IDE试验的2年数据也与先前结果一致,显示DCB组事件和重复干预更少。其他几项比较DCB与POBA的研究显示DCB的血管造影和临床结局更优。图3说明了AGENT DCB用于ISR的成功应用。
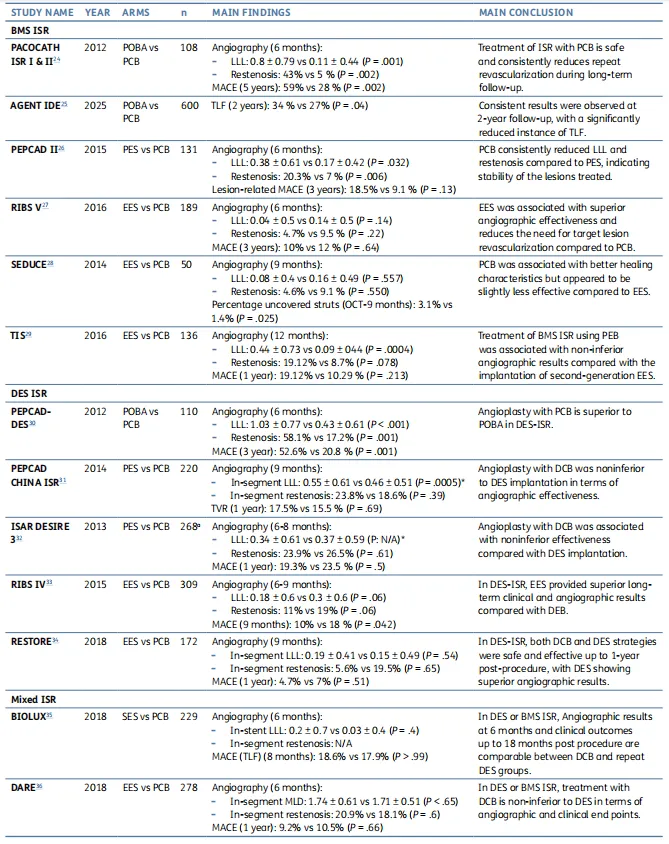
表1 使用药物涂层球囊(DCB)治疗冠状动脉支架内再狭窄(ISR)的主要随机临床试验总结BMS:裸金属支架;DCB:药物涂层球囊;DES:药物洗脱支架;EES:依维莫司洗脱支架;LLL:晚期管腔丢失;MACE:主要不良临床事件;MLD:平均管腔直径;ISR:支架内再狭窄;OCT:光学相干断层扫描;PCB:紫杉醇涂层球囊;PES:紫杉醇洗脱支架;POBA:普通球囊血管成形术;SCB:西罗莫司涂层球囊;SES:西罗莫司洗脱支架;TLF:靶病变失败;TVR:靶血管血运重建*注:在紫杉醇洗脱支架(PES)与紫杉醇涂层球囊(PCB)的晚期管腔丢失头对头比较中,未计算P值。
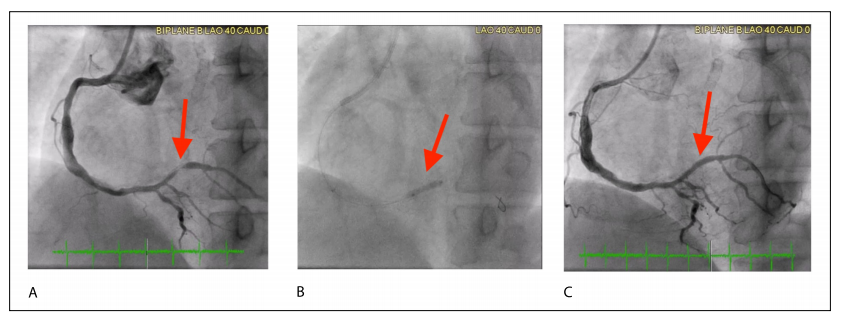
图3 冠状动脉造影图像展示使用药物涂层球囊(DCB)治疗支架内再狭窄(ISR)。(A) 术前图像显示靶血管存在90%的ISR。(B) 术中释放2.5 × 15 mm的AGENT药物涂层球囊,以6个大气压扩张60秒。(C) 术后图像显示DCB干预后ISR完全缓解,狭窄率为0%。
DAEDALUS研究(药物洗脱支架和药物涂层球囊血管成形术对冠状动脉支架内再狭窄发生的抗再狭窄有效性差异)是一项大型、研究者发起、协作性、个体患者数据荟萃分析,包括10项RCTs,比较DCB血管成形术与重复DES支架植入治疗冠状动脉ISR。在3年随访时,重复DES支架植入在减少TLR需求方面比DCB血管成形术适度更有效。此外,治疗效应与再狭窄支架类型之间存在显著交互作用,在DES-ISR患者中差异更大,而在BMS-ISR患者中效果相当。另一方面,在主要安全性终点(全因死亡、心肌梗死或靶病变血栓形成的复合终点)方面无显著差异,DCB组该结局发生率数值上更低。
亚组分析显示治疗效应与用于治疗ISR的DES代次之间存在显著相关性,与第一代DES相比,DCB相关事件发生率更低,而DCB与第二代DES之间效应相似。此外,最近来自SCAAR(瑞典冠状动脉造影和血管成形术注册表)的全国性长期分析显示与DAEDALUS研究相似的结果,其中DCB与DES相比TLR率更高。然而,BMS-ISR和DES-ISR之间的亚组分析显示DES和DCB在TLR和主要不良心脏事件(MACE)方面无显著差异。因此,DCB在治疗BMS-ISR时与重复DES支架植入同等有效和安全,但在治疗DES-ISR时效果不如重复DES支架植入。基于此,2024年欧洲心脏病学会/欧洲心胸外科协会慢性冠状动脉综合征管理指南更新,并推荐重复DES支架植入 over DCB用于治疗DES-ISR,具有I类A级推荐。
尽管DAEDALUS研究结果显示DCB在DES-ISR中劣于DES,但DCB的结局可能因再狭窄组织和原始支架特征的差异而异。在真实世界实践中,特定解剖和临床情况可能仍倾向于DCB方法。例如小血管尺寸、支架扩张不足、复杂分叉伴侧支从ISR段发出、或多个先前植入支架层等情况可能限制额外DES的效用。
尽管新一代DES支架可能略微减少ISR病变的TLR需求,但额外支架层的风险使得DCB在球囊血管成形术后实现充分病变准备时成为BMS-和DES-ISR的首选。此外,可能受益于较短DAPT持续时间的患者可能更适合DCB治疗。因此,患者特定因素可能影响结局,并应指导治疗方式选择,由操作者判断并针对患者解剖和临床概况。然而,需要针对不同临床和解剖情况设计良好、以临床终点为效力、具有长期临床随访的研究来优化DCB在ISR中的作用。
头对头比较不同DCBs的研究显示在血管造影和主要临床终点方面无显著差异。此外,一些重要措施可能提高DCB在ISR中的治疗效力,例如考虑DCB与其他设备联合治疗、适当病变准备、以及使用血管内成像和冠状动脉生理学。血管内超声或光学相干断层扫描的血管内成像可以提供对ISR潜在机制的见解,目前具有II类A级推荐。识别病变特异性贡献机械因素可以影响DCB与DES治疗ISR的决策。因此,DCB使用前血管内成像引导的病变准备,使用非顺应性球囊、切割球囊和高压球囊进行积极预扩张,可以优化DCB效果。钙化修饰工具如旋磨、旋转斑块切除术、血管内碎石术、以及评分或切割球囊可能是改善支架扩张和管腔增益、避免预扩张球囊滑动的辅助工具。
超适应症应用
目前,DCBs主要适用于治疗BMS和DES ISR。然而,新出现的证据表明将其应用扩展到其他适应症,如de novo冠状动脉疾病、分叉病变和弥漫长病变。DCBs也可能考虑用于糖尿病患者、急性冠状动脉综合征患者或高出血风险患者。图4和图5包括DCB在冠状动脉疾病中的适应症和治疗策略。
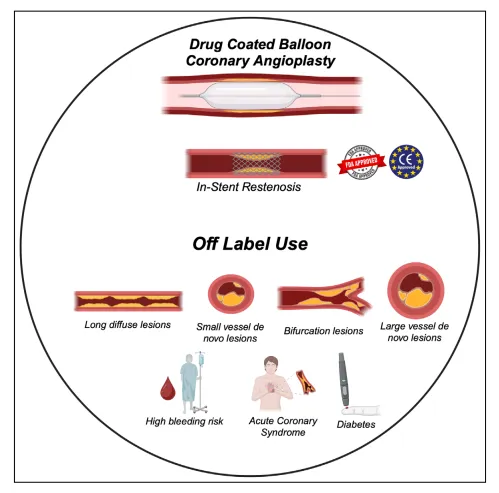
图4 药物涂层球囊冠状动脉成形术的适应症。
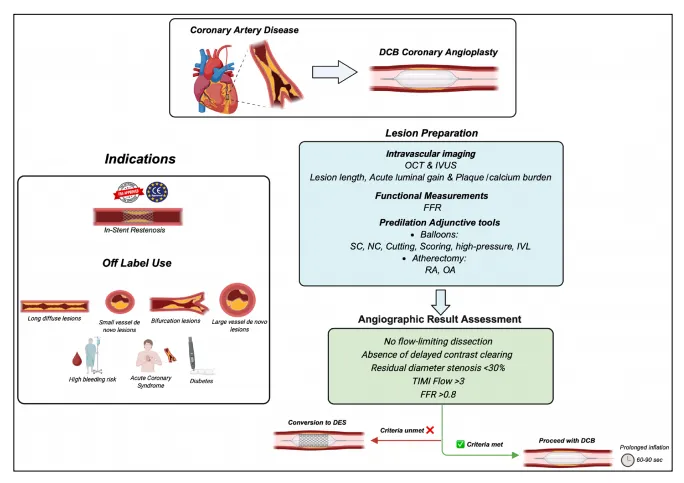
图5 核心图示: 药物涂层球囊在冠状动脉疾病中的适应症及治疗策略。(依据国际DCB共识小组文件改编)DCB:药物涂层球囊;DES:药物洗脱支架;FFR:血流储备分数;ISR:支架内再狭窄;IVL:血管内碎石术;IVUS:血管内超声;NC:非顺应性球囊;OCT:光学相干断层扫描;OA:轨道旋切术;PCI:经皮冠状动脉介入治疗;RA:旋转旋切术;SC:半顺应性球囊
以下部分探讨DCB使用的各种超适应症应用,突出支持其更广泛应用的日益增长证据
De Novo 大血管冠状动脉疾病
当治疗大口径冠状动脉疾病血管(LV-CAD),直径≥3.0 mm时,DESs传统上是首选选项,因为它们能够提供对血管壁的增强支持。然而,最近研究显示DCBs也是一个可行的治疗选项。DEBUT(稳定和不稳定心绞痛中的药物洗脱球囊:一项随机对照非劣效性试验)和PEPCAD-NSTEMI(冠状动脉疾病中紫杉醇洗脱PTCA球囊导管治疗非ST段抬高心肌梗死)试验分别在高出血风险患者和急性冠状动脉综合征患者中显示DCB和金属支架(BMS/DES)组间相似结局(TLF和MACE)。需要注意的是,NSTEMI试验报告DCB组有15%的额外支架放置发生率,突出由于DCBs引起的不可避免并发症,如冠状动脉夹层,可能需要“补救”支架植入。然而,另一项回顾性研究报道,虽然LV-CAD病变中冠状动脉夹层发生率为28.3%,但仅0.5%的病例需要补救支架植入,表明大多数DCB诱导的夹层是可控的,可以通过药物管理。
此外,DCB在LV-CAD中的使用已在各种临床背景下研究。SPARTAN DCB试验和Merinopoulos等人的另一项回顾性研究显示,在稳定CAD背景下治疗LV-CAD时,主要DES和DCB在全因死亡率方面无显著差异,分别在5年和3.6年随访时。Merinopoulos等人发现ST段抬高心肌梗死(STEMI)患者中DCB-only和DES-only组间结局相似——全因死亡率、净心脏事件(TLF、心血管死亡率、后续急性冠状动脉综合征、CVA、TIA和主要出血)在3年时。此外,REVELATION(急性心肌梗死中紫杉醇涂层球囊血管成形术与药物洗脱支架血运重建)试验评估了DCB血管成形术与DES在120名呈现STEMI且成功预扩张后残余狭窄<50%的患者中的安全性和有效性。在2年随访时,两组间MACE无显著差异。此外,DCB策略在9个月时分数流储备(FFR)评估方面非劣效于DES(DCB组[n=35]为0.92±0.05,DES组[n=38]为0.91±0.06;P=.27)。尽管DCBs作为LV-CAD单药治疗引起兴趣,但需要大型随机临床试验比较DCB与DES金标准以确认其有效性和安全性。
De Novo 小血管冠状动脉疾病
小血管冠状动脉疾病通常定义为血管直径<3.0 mm。在此类小血管中植入支架时出现缺点,因为随时间推移晚期管腔丢失变得更不利,导致更高ISR和不良事件率。来自单臂PEPCAD(紫杉醇洗脱PTCA球囊导管治疗小血管冠状动脉疾病)研究的早期结果提示安全性和有效性有利,12和36个月时心脏死亡、靶血管心肌梗死或TLF发生率低。
PICCOLETO(小冠状动脉血管PCI期间紫杉醇涂层球囊与药物洗脱支架)试验显示了对比结果,在6个月随访时,与DES相比,DCB显示出更高的百分比直径狭窄。
在小血管冠状动脉疾病最佳治疗策略存在不确定性的背景下,关键的BELLO(球囊洗脱和晚期丢失优化)试验提供了重要见解。这项对182名患者的随机研究比较了DCB血管成形术与紫杉醇洗脱支架(PES)植入术。
在6个月时,DCB在减少晚期管腔丢失方面既表现出非劣效性,也表现出统计学优效性(0.08±0.38 mm vs 0.29±0.44 mm;非劣效性P<.001,优效性P=.001),尽管有显著的20%的补救性BMS植入率。在24个月时,DCB组全因死亡、心肌梗死或靶血管血运重建的累积发生率显著低于PES组(14.4% vs 30.4%;P=.015)。到36个月时,DCB组的MACE显著降低(14.4%) versus PES(30.4%;P=.015),这强化了在选定的患有小血管疾病的患者中采用无支架策略的长期临床获益。
RESTORE SVD(药物涂层球囊与药物洗脱支架治疗小血管疾病)试验将230名患有de novo小血管冠状动脉疾病的患者随机分组,接受紫杉醇涂层球囊血管成形术或第二代佐他莫司洗脱支架治疗。在9个月时,DCB组在段内直径狭窄这一主要终点上不劣于DES组(29.6%±2.0% vs 24.1%±2.0%;非劣效性P<.001)。然而,与DES组相比,DCB组的段内最小管腔直径更小(1.40±0.42 mm vs 1.71±0.39 mm;P<.001),晚期管腔丢失率相似(0.25±0.42 mm vs 0.27±0.36 mm;P=.73)。在12个月和24个月时,复合临床结局没有显著差异。
一项来自瑞典冠状动脉造影和血管成形术注册中心(SCAAR)的大规模观察性分析,包括了14,778名连续接受紫杉醇涂层球囊(PCB)或第二代DES治疗的de novo小血管冠状动脉疾病患者,报告了相反的发现。在三年时,PCB组临床显著再狭窄的风险显著高于DES组(调整后HR, 2.03; 95% CI, 1.54-2.67)。相比之下,靶病变血栓形成的发生率在两组之间没有显著差异(调整后HR, 0.74; 95% CI, 0.41-1.33)。同样,在全因死亡率或心肌梗死率方面也未观察到显著差异。
关于DCB治疗de novo小血管CAD疗效报告的不一致,以及多个试验结果的不一致,可能归因于不同DCB技术之间缺乏类效应,以及手术技术的差异,特别是病变准备不充分。例如,PICCOLETO(药物洗脱球囊治疗小冠状动脉血管疾病疗效)研究中相互矛盾的发现可以部分解释为大约75%的入组患者存在次优的病变预扩张。表2提供了DCB在de novo小血管冠状动脉疾病中的主要RCTs总结。图6和图7说明了我们成功应用AGENT DCB治疗de novo小血管CAD的案例。
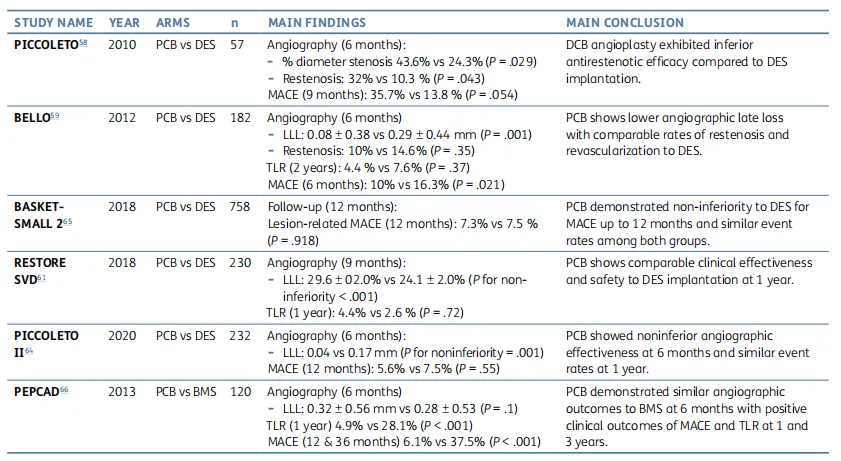
表2 新发小血管冠状动脉疾病中使用药物涂层球囊(DCB)的主要临床试验总结PCB:紫杉醇涂层球囊;DES:药物洗脱支架;MACE:主要不良临床事件;DCB:药物涂层球囊;LLL:晚期管腔丢失;TLR:靶病变血运重建;BMS:裸金属支架
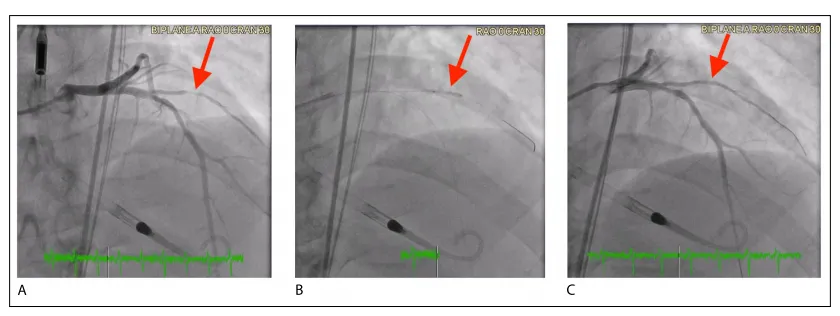
图6 应用药物涂层球囊(DCB)治疗新发小血管病变的冠状动脉造影图像示意图(A) 术前图像显示第一对角支近端段存在90%狭窄。(B) 术中释放2.5 × 15 mm的AGENT药物涂层球囊,以8个大气压扩张60秒。(C) 术后图像显示DCB干预后狭窄显著改善,残留狭窄率为20%。
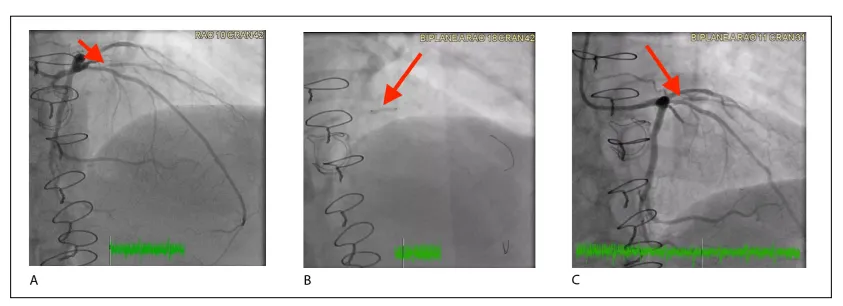
图7 冠状动脉造影图像展示使用药物涂层球囊(DCB)治疗累及第一对角支开口处、狭窄程度达90%的原发小血管病变。(A) 术前图像显示第一对角支开口处存在90%狭窄。(B) 术中释放2.5 × 12 mm的AGENT药物涂层球囊,以4个大气压扩张60秒。(C) 术后图像显示DCB干预后狭窄程度改善至30%,血管通畅性显著提升。
分叉病变
分叉病变是冠状动脉介入治疗中的一个重大挑战,占病例的15%至20%。这些病变尤其难以处理,因为分支血管闭塞、再狭窄和支架内血栓形成等并发症的风险更高。传统的双支架植入术治疗冠状动脉分叉病变并未显著改善结局,并可能增加住院率和MACE发生率。最广泛使用的方法仍然是在主支中进行单支架跨越植入,必要时对边支进行球囊扩张或临时支架植入。
单支架植入仍然是治疗分叉病变的主要方法,但它存在损伤边支的风险。POBA为扩张边支血管而不改变主支结构提供了一种替代方案。然而,在主支支架植入后仅对边支血管进行球囊PCI仍然导致两个分支的高再狭窄率。DCB保留了POBA的优点,同时提供了增强治疗效果的潜力,特别是对于小尺寸的边支血管。
过去十年的几项研究显示了使用主支临时支架植入和边支DCB治疗分叉病变的有希望的结果,如表3所述。
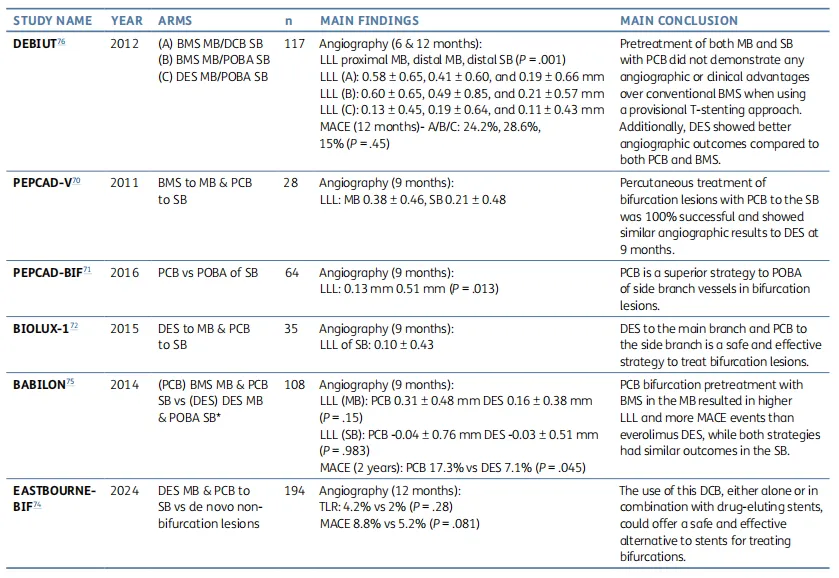
表3 药物涂层球囊(DCB)应用于冠状动脉分叉病变的主要临床试验总结BMS:裸金属支架;MB:主支;DCB:药物涂层球囊;SB:边支;POBA:普通球囊血管成形术;DES:药物洗脱支架;LLL:晚期管腔丢失;MACE:主要不良临床事件;PCB:紫杉醇涂层球囊;TLR:靶病变血运重建*注:在BMS主支组中,主支采用紫杉醇涂层球囊(PCB)进行预扩张。
BABILON(分叉病变中的紫杉醇涂层球囊)试验将108名冠状动脉分叉病变患者随机分组,一组在两个分支中顺序进行DCB血管成形术预扩张,然后在主支中临时植入BMS;另一组采用标准方法,即预扩张后在主支中临时植入依维莫司洗脱支架。在9个月时,DCB加BMS策略在段内晚期管腔丢失方面显示出不劣于单独DES策略(0.31±0.48 mm vs 0.16±0.38 mm;非劣效性P<.001,优效性P=.15)。边支晚期管腔丢失在组间具有可比性(-0.04±0.76 mm vs -0.03±0.51 mm;P=.983)。然而,DCB组在9个月时经历了显著更高的TLR率(13.5% vs 1.8%;P=.027),主要由主支的再狭窄驱动,并且在MACE方面无统计学显著性。
DEBIUT(分叉病变试验中的药物洗脱球囊)研究显示了相互矛盾的证据,其中6个月血管造影随访显示,基于DCB的策略与基于BMS的策略相比没有显著差异,并且被发现效果不如基于DES的策略。
另一项试验侧重于DCB血管成形术在DES植入主支后治疗边支的潜在益处。9个月的随访显示DCB组结果更好,其中病变内晚期管腔丢失更低(0.13±0.31 mm vs 0.51±0.66 mm;P=.013),最小管腔直径更大(1.78±0.37 mm vs 1.39±0.80 mm;P=.015),并且接受DCB治疗的患者二元再狭窄发生率更低(5.9% vs 25.7%;P=.045)。
BIOLUX-I研究评估了主支植入DES联合边支使用DCB的策略,结果显示边支晚期管腔丢失为0.10±0.43 mm,表明这是一种安全有效的治疗分叉病变的方法。
EASTBOURNE-BIF研究的最新数据显示,在主支植入DES并边支使用DCB的策略与de novo非分叉病变相比,在12个月时TLR(4.2% vs 2%;P=.28)和MACE(8.8% vs 5.2%;P=.081)无显著差异,支持DCB作为治疗分叉病变的可行选择。
随着支持在分叉病变中使用DCB的证据不断增多,其在该适应症中的常规应用可能在日常实践中变得更加普遍。然而,仍然需要更稳健和高质量的证据来确立其最佳使用方案。
弥漫长病变
支架长度和负荷(支架数量)是ISR和支架内血栓形成的预测因素。这直接适用于弥漫长病变。这种特定的冠状动脉表型需要使用长支架甚至重叠支架,这两者都与损害长期支架完整性的风险增加有关。因此,使用纯DCB策略或DES与DCB混合方法可以通过降低支架长度和总支架负荷来提供更安全、更广泛的治疗选择。
HYPER研究评估了DCB和DES混合方法在de novo弥漫性冠状动脉疾病中的疗效,结果显示在1年时心脏死亡、靶血管心肌梗死和缺血驱动的靶病变血运重建发生率较低,支持这种联合策略的可行性。
Gitto等人的研究表明,基于DCB的方法能够避免近三分之一的病例植入支架,在2年随访时,DCB±DES组和纯DCB组之间的事件发生率相似(MACE=20.8% vs 22.7%,P=.74)。
一项前瞻性观察性研究发现,对于平均长度为44 mm的长病变,接受单独DCB或联合DES治疗的患者实现了可比的3年TLR率或MACE。值得注意的是,DCB组未观察到血栓形成病例,而在DES治疗队列中报告了四例支架内血栓形成。
当前数据表明DCB在治疗弥漫长病变方面具有前景。未来的研究可能会进一步阐明DCB和DES联合治疗弥漫长病变的益处,特别是在优化患者选择和病变准备策略方面。
临床综合征 急性冠状动脉综合征急性冠状动脉综合征与血栓形成和PCI并发症风险升高相关,这可以通过急性期血管壁动态变化(主要是血管收缩和斑块重塑)来解释。因此,在直接PCI病变中,尤其是在血栓负荷高的情况下,通常优选延迟支架植入而非立即植入。
PEPCAD-NSTEMI试验显示,在210名NSTEMI患者中,纯DCB策略在9个月时复合终点(心脏死亡、心肌再梗死或靶病变血运重建)的发生率方面不劣于BMS或DES植入(3.8% vs 6.6%;非劣效性P<.003)。
REVELATION试验在STEMI患者中比较了DCB与DES,结果显示在2年随访时,复合终点(全因死亡、复发性心肌梗死或靶病变血运重建)发生在DCB组5.4%和DES组1.9%(HR, 2.86; 95% CI, 0.30-27.53; P=.34)。
一项包括三项随机试验和一项观察性研究的荟萃分析显示,在急性心肌梗死患者中,DCB与DES在9个月时的MACE、全因死亡率、心脏死亡、心肌梗死和TLR发生率相似,晚期管腔丢失也相当。
这些发现可能促进DCB在急性冠状动脉综合征患者中的使用,但需要谨慎,因为试验参与者是经过精心挑选的,结果可能无法反映真实世界的情况。
双联抗血小板治疗与高出血风险根据当前欧洲指南,对于非高出血风险(HBR)患者,DCB血管成形术后建议的DAPT持续时间是:稳定型冠状动脉疾病患者为6个月,急性冠状动脉综合征患者为12个月。对于HBR个体,较短的3个月DAPT持续时间被认为是合适的(IIa类),1个月方案被视为可能的选择(IIb类)。
DEBUT试验显示,在高出血风险患者中,DCB联合1个月DAPT在减少心血管死亡、非致命性心肌梗死或缺血驱动的TLR方面优于BMS(1% vs 14%;RR, 0.07)。一项观察性研究显示,在1,025名接受纯PCB血管成形术治疗的患者中,1个月DAPT方案在9个月时缺血事件发生率较低(心脏死亡1.3%;心肌梗死3.4%;靶病变血栓形成0.8%)。
专家共识认为,DCB血管成形术后1个月的DAPT持续时间可能足以安全预防血栓并发症。尽管新一代DES允许HBR患者考虑1至3个月的DAPT,但DCB血管成形术后极低的抗血栓需求使其成为HBR患者的一个有吸引力的选择。
糖尿病DCB在糖尿病患者中显示出治疗ISR和de novo小血管CAD的潜力。糖尿病人群由于代谢异常,再狭窄和不良结局风险更高,DCB的”不留异物”方法可能提供优势。
研究显示,在小血管CAD糖尿病患者中,DCB与DES在短期疗效和安全性方面相当。一项荟萃分析表明,DCB在高危患者和糖尿病患者中具有可接受的安全性和有效性。
目前的证据支持DCB在改善糖尿病患者血管造影和临床结局方面的潜力,但需要更多随机对照试验来明确其长期疗效和安全性。
病变准备的重要性成功的DCB治疗高度依赖于充分的病变准备。血管内成像(如OCT或IVUS)对于评估病变特征至关重要。积极的病变预处理,包括使用非顺应性球囊、切割球囊或评分球囊,可以提高DCB的效果。
钙化病变需要专门的修饰工具,如旋磨、轨道斑块切除术或血管内碎石术,以优化管腔增益。DCB输送时,球囊与血管比率应在0.8-1.0之间,膨胀时间至少60秒,以最大化药物输送。
尽管DCB可能引起冠状动脉夹层,但大多数情况下不会限制血流,且通常不需要干预。然而,操作者需要识别这种并发症的可能性,因为它可能需要补救性支架植入。
关键要点
1.药物涂层球囊为冠状动脉支架提供了可行的替代方案。其采用”不留异物”的策略,既能减少对永久性支架的需求,又可降低再狭窄、血栓形成及长期缺血事件的风险。
2.在治疗冠状动脉支架内再狭窄方面,药物涂层球囊疗效显著:相较于普通球囊血管成形术具有更优的临床结果,在处理支架内再狭窄时与药物洗脱支架表现相当。
3.其冠状动脉介入适应症正不断拓展:最新证据表明,除支架内再狭窄外,该技术在原发冠状动脉病变、小血管病变、分叉病变及长弥漫性病变等复杂病例中也展现出广阔应用前景,临床疗效令人鼓舞。
4.对高出血风险患者尤为有利:可缩短双联抗血小板治疗周期;研究证实其对糖尿病患者以及急性冠脉综合征低危病变患者的疗效不劣于支架植入。
5.成功应用的关键在于精细的病变预处理:除血管内影像引导外,常需配合高压球囊、切割球囊等先进器械,必要时进行钙化修饰,以此优化药物输送效果并降低血管夹层等并发症风险。
结语总结
DCB作为冠状动脉介入治疗的一种方法显示出巨大潜力,特别是在ISR治疗中表现出色。其在de novo病变、小血管疾病、分叉病变和弥漫长病变等复杂情况中的应用正在扩展。DCB的主要优势在于其”不留异物”策略,减少了长期支架相关并发症的风险,特别适合高出血风险患者和需要短程DAPT的患者。
然而,最佳结果依赖于适当的患者选择、充分的病变准备和精确的操作技术。虽然现有证据支持DCB在多种临床情况下的应用,但仍需要更多大规模随机试验来确立其在非ISR病变中的标准治疗地位。未来的研究应着重于优化DCB技术、确定最佳适应症以及开发标准化使用协议,以充分发挥这种有前景技术的潜力。
文章来源:NVVIMed。文章内容仅供知识交流分享使用,如涉侵权请联系我们删除