2026年上海医疗器械设计与制造展发现脉冲场消融通过施加短时间的高压电脉冲(波形),以不可逆电穿孔(IRE)的方式在心肌组织形成非热消融灶。在第一代脉冲场消融系统的市场化竞速中,导管研发多围绕波形和电压展开,而导管结构、电极配置及能量传递的底层生物物理学原理未得到应有的重视。近日,《PCAE》上的一篇文章重新梳理脉冲场消融的基本原理,探索如何通过理解电场行为、接触压力和能量的空间分布,开启脉冲场消融技术的下一轮创新。

一、第一代 PFA 为何成功?又为何需要优化?
1. 第一代 PFA 的核心成功逻辑:突破射频消融(RF)的固有约束
PFA 作为非热消融技术,以不可逆电穿孔(IRE)为核心机制,相比传统 RF 消融,从设计上摆脱了诸多技术限制,成为其快速临床落地的关键:
(1)操作门槛大幅降低无需 RF 消融要求的精准逐点施术、严格接触力控制和持续灌洗控温,减少术者操作负荷和认知压力,缩短手术时间;
(2)安全性优势
心肌组织选择性消融,降低心肌穿孔、膈神经热损伤、食管热损伤等风险,无需膈神经起搏、食管温度监测等附加步骤;
(3)导管设计更灵活
可采用大头端、多电极导管设计,提升导管消融时的稳定性,且无需依赖导管偏转,简化设计并降低制造成本;
(4)能量传递更高效
消融时间短,无需长时间保持导管稳定接触,同时消除了 RF 消融的实时热管理的需求。
2. 第一代 PFA 的核心短板:研发重心的偏移与设计误区
第一代 PFA 研发为快速上市,将核心精力放在波形设计和电压参数上,却忽视了导管形态、电极配置、能量传递的生物物理特性等关键维度,导致临床出现消融灶精度不足、耐久性欠佳、非靶组织安全性风险等问题,且早期部分设计假设被临床证伪(如 “PFA 无需严格的组织接触”,实际组织接触是 PFA 有效消融的核心前提)。这一短板也导致第一代 PFA 虽临床普及快,但在临床试验中尚未展现出优于 RF 消融的长期临床结局,成为下一代导管设计需要解决的核心问题。
二、下一代脉冲场消融设计与工程学要求
高压、非热的能量传递特性,以及对手术安全性、可重复性、三维系统整合的需求,为脉冲场消融技术带来了新的设计和工程学挑战。脉冲场消融发生器的设计发生了重大转变:需向多个电极递送极短的高压脉冲序列,部分场景下要求微秒级的精准度。此外,发生器必须能在非最佳条件下(如导管仍在鞘管内、电极重叠或靠近金属部件导致短路时)检测并阻断能量传递。高电流和高电压会放大这些风险,因此相较于射频消融系统,脉冲场消融对安全阈值和防护策略提出了不同的工程学要求:如采用更大的电极表面,在高压下实现均匀电场传递,同时降低电流密度,减少局部发热;导管杆体和延长电缆采用先进的绝缘材料,对传感器进行防护并对电路做屏蔽处理等等。
三、PFA 能量递送的核心生物物理原则:导管设计的底层逻辑
这是本文的核心理论部分,所有导管设计的优化均基于此,也是理解 PFA 消融灶形成的关键。
1. 组织接触是 PFA 安全有效消融的第一前提
心肌组织(高电阻)和血液(高导电性)的电导率差异,直接决定电场分布和消融效果:无组织接触时,电流多经血液流失,心肌内电场强度不足,无法实现 IRE;
有效组织接触时,电路被迫通过高电阻的心肌,提升局部电场强度,实现有效 IRE;
电场强度随与电极距离非线性快速衰减,因此电极间距、取向、组织接触的精准控制,是兼顾靶组织消融和周围组织保护的关键。
(1)电流易向血液传导
当脉冲场消融导管电极未与靶组织接触时,大部分电流会通过血液传导,导致心肌内电场强度不足,无法实现不可逆电穿孔;
(2)组织接触使电场局部化
当导管头端与靶组织形成有效接触时,电路被迫通过高电阻的心肌组织,使局部电场强度升高,从而实现有效的不可逆电穿孔;
(3)电场强度随距离衰减
电场强度呈非线性衰减,因此必须通过可控的电极间距、取向和组织接触,确保靶组织获得足够的电场强度,同时保护周围组织;
(4)阻抗影响峰值电流
电流受组织、血液和导管组件的综合电阻影响。尽管发生器输出固定电压的脉冲,但高阻抗会减少向组织递送的电流,使电场更局部化;反之,低阻抗会导致峰值电流升高。电流的分配比例(即流经组织和血液的电流占比)最终决定消融灶的形成、热负荷和能量效率;
(5)焦耳热仍为影响因素
尽管脉冲场消融属于非热消融技术,但高压短脉冲仍会在电极界面产生电阻性发热。阻抗和电流大小的变化,直接影响能量递送过程中的产热量。脉冲场消融产生的焦耳热持续时间短、仅存在于组织表层,不足以向深层传导并造成显著的热损伤。
2. PFA 并非 “无热”,而是 “非热损伤为主”,需主动控热
尽管 PFA 的核心损伤机制是 IRE 而非热损伤,但高压脉冲会在电极界面产生短暂的焦耳热,反复消融可能导致热量累积,引发溶血、局部组织热损伤等问题,因此需通过设计和操作策略控热:
电压阈值设定:略高于电穿孔阈值,兼顾 IRE 效果和最小化多余电流;
脉冲间延迟 / 导管重定位:消散残余热量,低血流区域(如左房后壁)需主动重定位;
电极短接:增大电极表面积,降低电流密度和热集中;
灌注设计:冷却电极、冲走血液,减少局部加热和溶血。
3. 电场强度的平衡:心肌选择性与非靶组织安全的博弈
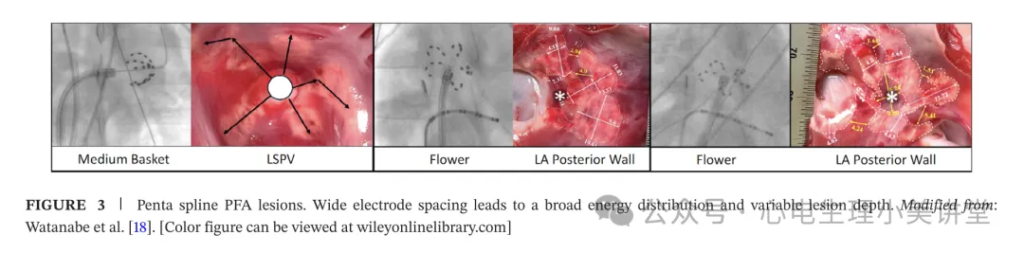
PFA 的心肌选择性源于心肌细胞的电穿孔致死阈值远低于其他组织(人心室肌仅 416 V/cm,而食管平滑肌 / 血管内皮约 1750 V/cm,红细胞 1500-2000 V/cm,周围神经约 3800 V/cm),临床常用 PFA 电压(最高约 2000 V)正是为了突破心肌阈值并实现透壁消融。但该电压已接近红细胞、食管平滑肌等组织的阈值,电极界面的强电场易导致红细胞意外电穿孔(溶血),而电场的快速衰减成为天然的 “安全缓冲”—— 这进一步强调了电极空间分布和组织接触控制的重要性:确保靶组织电场足够,同时让周围组织处于电场衰减后的安全范围。
4. 消融灶耐久性的关键:将 “可逆损伤区” 转化为 “不可逆消融区”
PFA 消融后会形成两个区域:不可逆消融区(电场强度达 IRE 阈值,心肌细胞死亡,是形成耐久性消融灶的核心;)和可逆电穿孔区(电场强度不足 IRE 阈值,仅造成心肌细胞短暂兴奋性丧失,无 ECG 信号,但细胞可恢复,无法形成持久消融。)同一解剖位点的重复消融是将可逆电穿孔区转化为不可逆消融区的核心策略,也是提升消融灶耐久性、实现肺静脉持久隔离的关键。
5. 广谱式与聚焦式消融(Broad Versus Focused Lesions)
基于上述原理,目前形成了广谱式和聚焦式两种能量传递方式,分别对应不同的导管几何结构和手术流程,具体如下:
(1)聚焦式传递(Focused delivery)
以VARIPULSE为例, 这类导管采用电极间距固定的紧密排列的电极,能量更聚焦,也最可控,通过重复消融,最小化可逆电穿孔区域,提升病灶的持久性。因此,聚焦式能量传递系统允许以一致的电场方向重复施加相同优化序列,从而确保可预测性并形成均匀病灶。
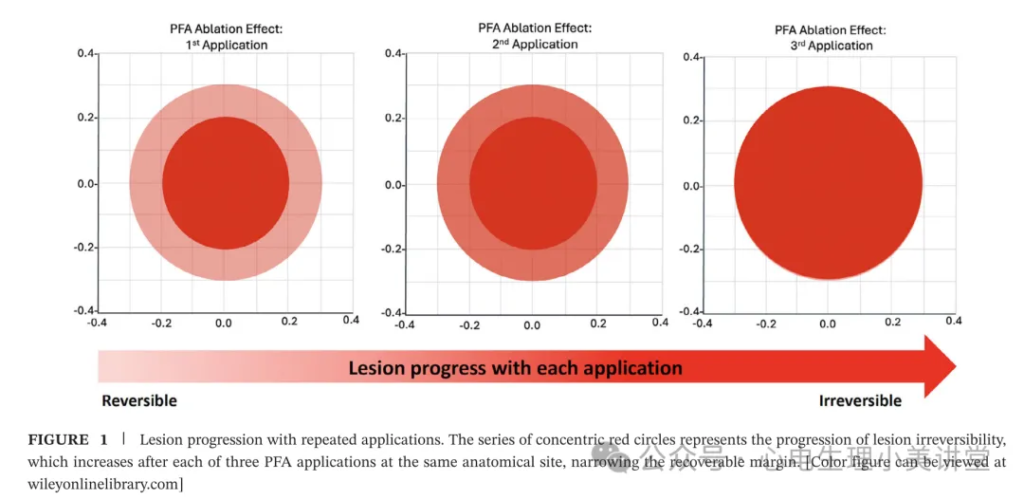
(2)广谱式传递(Broad delivery)
以FARAWAVE 等系统(花型、篮型、橄榄型)为例,其可形成更大的消融灶范围,导管操作的灵活性更高。该方式虽天然会产生更广泛的可逆电穿孔区,但可通过重复消融和变换导管形态,从不同角度补充能量,将更多可逆区转化为不可逆区,确保组织的有效消融覆盖。
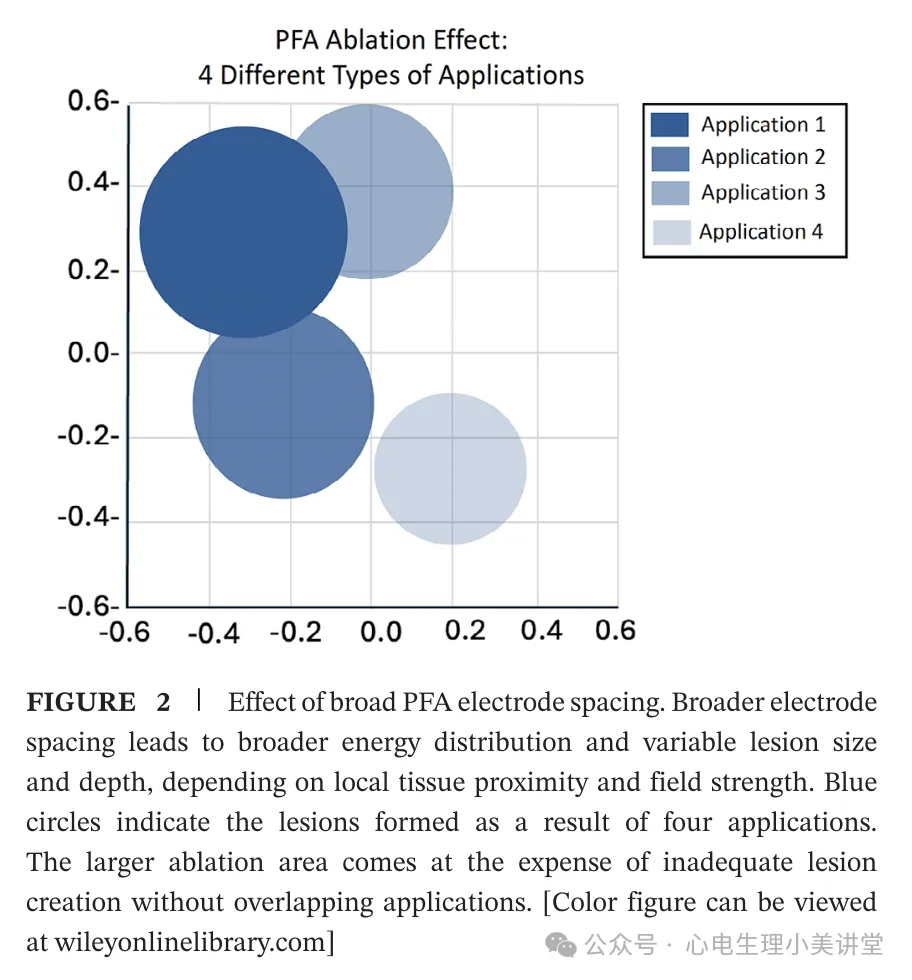
但电极间距过大会导致能量分布范围扩大,消融灶的大小和深度会随局部组织接触情况和电场强度发生变化(见图 2、图 3)。在此情况下,要形成持久性消融灶,每次消融需包含多个脉冲序列。这些序列有助于弥补导管定位过程中电极间距变化带来的的未知性、变异性及可能的电场方向偏差,但同时也会增加非靶区域的消融风险。相比之下,固定间距的设计能更好地保证电场均匀性,减少操作不确定性。归根结底,两种策略均旨在平衡操作便捷性与消融灶一致性。但肺静脉的持久隔离,不仅取决于波形特征,还同样依赖于能量的递送方式、聚焦位置和重复次数。
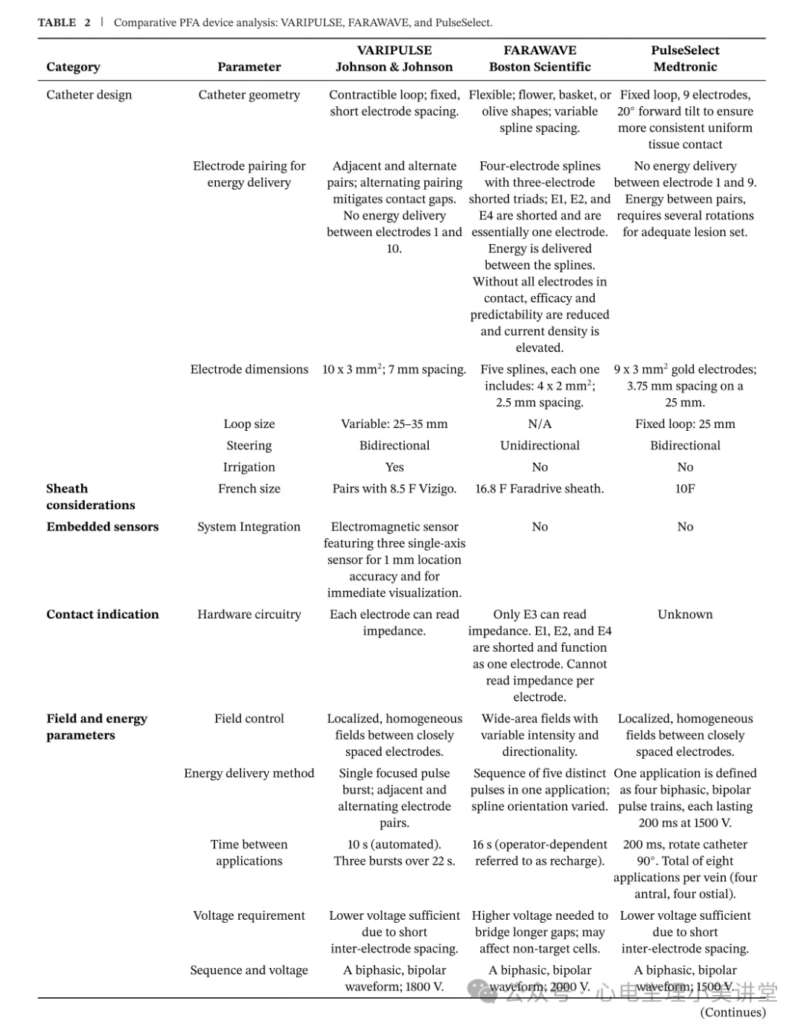
四、当前主流 PFA 导管系统对比:设计差异决定临床表现
本文重点对比了全球四大主流 PFA 导管系统(VARIPULSE / 强生、FARAWAVE / 波士顿科学、PulseSelect / 美敦力、Sphere-9 / 美敦力),核心差异集中在导管几何、电极配置、能量参数、消融灶特性四大维度,以下为核心对比结论:
1. VARIPULSE(强生):聚焦式能量传递的代表,精准性优先
核心设计:可收缩环型,固定短电极间距(7mm),10 个 3mm 电极,双向可调弯,带盐水灌洗和磁传感器(定位精度 1mm);
能量参数:双相双极波形,1800V,同一位点 3 次重复放电(自动化间隔 10s),相邻或者相间电极配对,1、10电极间无电场形成;
消融特点:消融灶可预测、深度均匀、透壁性好,可逆电穿孔区域较小,每根肺静脉至少 4 次消融;
安全优势:每个电极可监测阻抗(判断组织接触),盐水灌洗设计可降低热堆积,短电极间距降低电压需求,减少非靶效应。
2. FARAWAVE(波士顿科学):广谱式递送的代表,灵活性优先
核心设计:柔性多形态(花 / 篮 / 橄榄),五条臂宽间距电极,每条臂内电极短接(3 个电极合并为 1),单向操控,无盐水灌洗,仅 1 个电极可监测阻抗;
能量参数:双相双极波形,2000V,单次放电含 5 个不同脉冲序列,花瓣间递送能量,需每根肺静脉至少 4 次消融(2 种形态各 2 次);
消融特点:消融灶范围大、可逆损伤区广,深度不均,需多次放电补充,非靶组织安全性风险略高;
安全短板:电极短接导致电流密度升高,2000V 高压接近红细胞阈值,溶血风险较高,且无灌洗设计,热堆积风险增加。
3. PulseSelect(美敦力):轻量化聚焦式,低电压低功率
核心设计:固定环型(25mm),9 个 3mm 金电极,短间距(3.75mm),双向操控,无盐水灌洗,电极直径更小;
能量参数:双相双极波形,1500V(最低),单次放电为 4 个 200ms 脉冲序列,需每根肺静脉 8 次消融(旋转 90° 补gap);
消融特点:消融灶为半环形,需 “拼接” 实现环状阻滞,精准性较好,但电极直径小导致接触面积不足,需精准定位;
安全优势:低电压抵消了小电极带来的高电流密度风险,溶血风险低;不足是需多次旋转定位,操作步骤更多。
4. Sphere-9(美敦力):特殊的双能量设计,RF + 单极 PFA
核心设计:9mm 聚焦式网格篮型电极,原为 RF 消融导管改造,单极 PFA,带 9 个热电偶(温度 / 阻抗反馈);
能量参数:PFA 最高 57A 大电流,RF 为 73-75℃控温,网格结构有效接触面积小于标称直径;
消融特点:消融灶局限于接触位置,范围较小、深度较浅,依赖高密度消融,是唯一兼具 RF 和 PFA 的双能量系统;
核心问题:网格结构 + 单极 PFA 导致电流密度不均匀,组织接触需高压力,易引发组织黏连、血液凝固、蒸汽爆震,且多传感器仅 2-3 个接触组织,反馈不准确。

房颤肺静脉的持久隔离,不仅取决于波形,更取决于能量如何递送、聚焦何处、重复次数—— 聚焦式更适合追求消融精度和耐久性,广谱式更适合追求操作灵活性。
五、下一代 PFA 导管的设计优化方向:从 “参数迭代” 到 “系统工程”
基于第一代 PFA 的设计痛点和生物物理学原理,本文明确了下一代 PFA 导管的核心研发方向,核心是将 PFA 视为 “系统工程”,整合电场行为、接触动力学、空间能量分布,而非单纯优化波形和电压:
1、精准的组织接触控制
保留并优化阻抗监测、接触力传感等原 RF 时代的技术,适配 PFA 的生物物理需求,实现电极 – 心肌接触的实时精准监测;
2、电极的精细化设计
根据消融靶点(如肺静脉 / 心室)优化电极间距、直径、排布,兼顾电场均匀性、电流密度控制和消融覆盖范围,避免短接电极的高电流密度风险;
3、高压适配的工程设计
采用耐高压绝缘材料、重新设计连接器布局、增加快速开关架构,防止高压脉冲下的电弧、漏电、跨通道能量泄漏,同时保护传感器和辅助电路;
4、控热与抗溶血的一体化设计
整合灌注、电极短接、脉冲延迟等策略,从设计上最小化焦耳热累积和红细胞电穿孔,平衡高压需求和安全阈值;
5、消融灶的实时监测与个性化
结合三维标测、电磁定位、阻抗反馈,实现消融灶形成的实时可视化,根据组织厚度、解剖结构调整能量递送参数,实现个性化消融;
6、与标测系统的深度整合
将 PFA 导管与三维电生理标测系统融合,实现 “建模 – 标测 – 消融 – 验证” 的一体化,提升手术流程的效率和消融的精准性。
六、研究局限性
仅分析了四大主流厂商的产品,未覆盖新兴 PFA 导管设计;
缺乏针对不同心律失常亚型(阵发性 / 持续性房颤、室速)和解剖变异的精细化设计分析,相关长期临床数据仍在积累;
未深入探讨可逆电穿孔区的长期临床影响、AI 辅助三维建模等新兴技术的应用。
七、总结
本文的核心观点为:PFA 的临床潜力,不仅取决于电穿孔的非热机制,更取决于导管形态设计对能量递送的精准控制。第一代 PFA 凭借突破 RF 消融的操作和安全优势实现快速普及,但因研发重心偏移导致临床结局未达预期;而下一代 PFA 的核心突破点,在于回归 PFA 的生物物理学底层逻辑,通过导管形态、电极配置、能量递送策略的系统优化,实现消融灶精准化、耐久性提升、非靶效应最小化,最终让 PFA 从 “更安全的消融技术” 升级为 “更安全且更优效的消融技术”。八、研究结论
尽管脉冲场消融(PFA)通过克服传统射频消融(RF ablation)的局限性实现了快递普及,但在导管设计和改善临床疗效的等方面依然有提高的空间。通过重新审视PFA的底层逻辑,并融合电场形成、接触力等最因素,未来的导管设计有望进一步提高消融精准度,同时最大限度地减少非靶效应,从而提升新一代平台的安全性和有效性。
文章来源:心电生理小美课堂。文章内容仅供知识交流分享使用,如涉侵权请联系我们删除