法规质量
【学术分享】医疗器械经营企业在商品流通中的质量管理方式研究
医疗器械作为一种健康辅助性设备在当前的生活中被普遍的应用,关注医疗器械的质量对于使用者的生命健康安全而言有着重要的意义,所以医疗器械经营企业需要本着负责的态度做好商品的流通质量管理,这样,医疗器械的具体利用价值才会有更好的发挥。总结当前医疗器械经营企业在商品流通过程中的具体质量管理方式,分析这些管理方式的不足,并针对不足做具体的管理方式改进,这样,企业在管理中的具体措施利用会更加的科学,商品质量的控制效果也会更加显著。本文就医疗器械经营企业在商品流通中的智联管理方式做分析讨论,目的是为实践措施的采取提供指导。
2018年12月24日
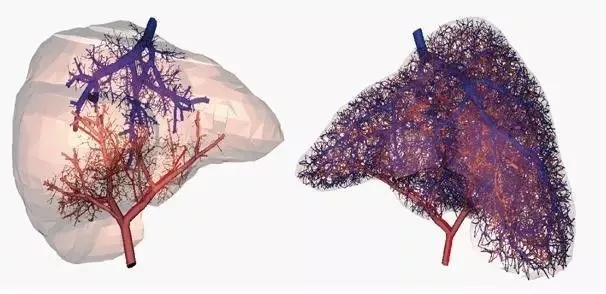
3D打印器官能否跨越技术与法规障碍,解决移植器官短缺问题?
器官移植是治疗部分器官衰竭患者的手段,仅在中国,脏器衰竭患者的器官移植需求量就达到了年均30万例。公开数据显示,2015年,中国成功完成肝脏移植2000多例、肾移植5367例,但2015年肝脏移植需求者新增4000多人,肾脏移植需求者新增了1万多人,供需…
2018年12月12日
【原创】关于医疗器械质量管理体系常见的文件理解
本文从医疗器械从业者本身出发,谈谈对医疗器械质量管理体系常见文件,如工艺规程、程序文件、作业指导书、标准管理规程、标准操作规程的理解,希望对初入门者有点帮助。
2018年12月7日
医疗器械上市将有新规!FDA将淘汰510(K)
FDA局长Scott Gottlieb博士和医学设备中心和放射卫生主任(CDRH )Jeff Shuren近日发表了一份声明关于改革FDA 510 (k)规定,让FDA审批路径能够跟上快速发展的复杂技术。
阅读更多
2018年12月7日
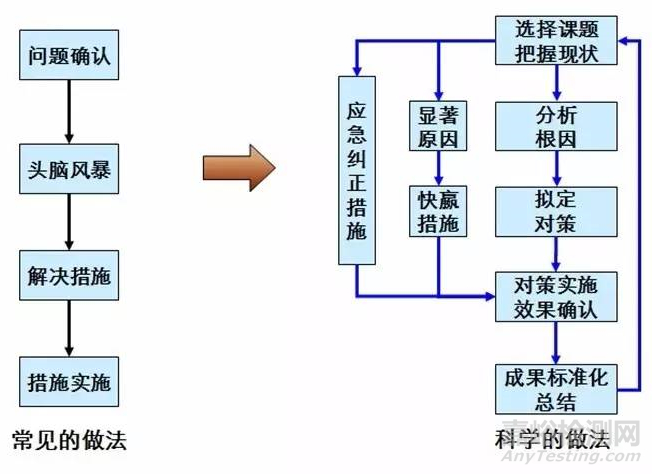
医械研发项目怎样做质量管理?
企业研发项目质量不仅直接影响项目本身的效益,其中的产出物质量将带入其后的生产运营中,对企业的产品、技术、效益、形象产生更为深远的影响。企业研发项目不仅具有一般项目所共有的目的性、独特性、一次性、制约性,更具有不确定性和高风险性。因此,在项目的实施过程中更应加强质量控制,通过质量投入来保证工作质量和产出物质量。
2018年11月22日
2018年11月22日